(15分)“优先反应思想”是一条重要的化学学科思想。根据所学知识及题目提供的相关数据,回答下列问题:
(1)向FeBr2溶液中滴加少量氯水,溶液变黄。你认为使溶液变黄的微粒其符号是用实验证明你的观点,简述实验操作及现象 。
(2)用惰性电极电解由等物质的量的NaBr,KI, NaCl组成的混合溶液,阳极首先发生的电极反应式是 。
(3)己知常温下一些电解质的相关数据见下表:
①向等物质的量浓度的Na2C03, CH3COONa, NaClO组成的混合溶液中逐滴加入稀硫酸,首先发生反应的离子方程式是 。
②向浓度均为0.010 mol/L的NaCl, Na2Cr04组成的混合溶液中逐滴加入浓度为0.010 mol-L -1AgN03溶液,首先生成的沉淀其化学式为 。
(4)分别向四份各100 ML,浓度均为2 mo1-L-1的FeC13溶液中,加入铁、铜组成的均匀粉末状混合物,得到如下数据:
①根据表中的数据可求出粉末中铁、铜的物质的量之比为 。
②根据表中的数据分析I反应后的溶液中存在的金属阳离子有〔用离子符号表示) 。
A(g)+2B(g)  2C(g)的反应中,时间t与C的体积分数(C%)的函数关
2C(g)的反应中,时间t与C的体积分数(C%)的函数关
系如图所示。回答下列问题:
(1)图A中若两条曲线分别表示在100℃和400℃时的C%与时间t的函数关系,则P表示的温度为℃,
从P、Q分析反应A(g)+2B(g)  2C(g)是反应(填“吸热”或“放热”);
2C(g)是反应(填“吸热”或“放热”);
(2)图B中P表示的温度为℃,反应A(g)+2B(g)  2C(g)是反应(填“吸热”或“放热”)。
2C(g)是反应(填“吸热”或“放热”)。
将固体NH4I置于密闭容器中,某温度下发生下列变化:
NH4I(s) NH3 (g) + HI(g) 2HI(g)
NH3 (g) + HI(g) 2HI(g)  H2(g) + I2(g)
H2(g) + I2(g)
当反应达到平衡时c(H2)=" 0.5" mol/L, c(HI)=" 4" mol/L, 则 c(NH3),HI 的分解率为。
反应m A+n B p C在某温度下达到平衡。
p C在某温度下达到平衡。
(1)若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、
n、p的关系是。
(2)若C为气体,且m + n = p,在加压时化学平衡发生移动,则平衡必定向______方向移动。
(3)如果在体系中增加或减少B的量,平衡均不发生移动,则B肯定不能为_____态。
在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)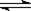 CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =。
(2)该反应为反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为℃。
(6分)依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g乙醇燃烧生成CO2和液态水时放热29.7kJ。则表示乙醇燃烧热的热化学方程式为_____________________________。
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热
量_________________________________。
(3)已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________________________________