(1)海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如下: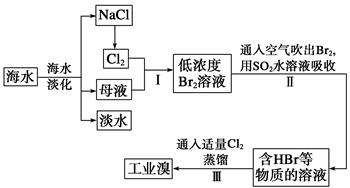
操作Ⅱ发生反应的离子方程式为____________________;
可以用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和-1价,操作Ⅲ中如果用稀硫酸代替氯气,则操作Ⅲ中发生反应的离子方程式为_________________。
(2)溴苯是一种化工原料,可以用溴和苯反应合成。实验室合成溴苯的装置示意图如下: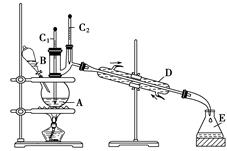

下表为苯、溴和溴苯的相关数据:
| |
苯 |
溴 |
溴苯 |
| 密度/g·cm-3 |
0.88 |
3.10 |
1.50 |
| 沸点/℃ |
80 |
59 |
156 |
| 水中溶解度 |
微溶 |
微溶 |
微溶 |
回答下列问题:
在A中加入30.0 mL无水苯和少量铁屑。在B中小心加入8.0 mL液态溴。向A中滴加液溴,反应一段时间后,点燃酒精灯加热蒸馏。
①A的容积最适合的是________(填编号)。
a.25 mL b.50 mL c.100 mL d.250 mL
②收集溴苯时,应根据________(填“C1”或“C2”)所显示的温度,其温度应为__________________。
③在反应开始后到收集溴苯之前,应先将F装置连接在D装置后,用它可承接的物质有___________(填化学式)。
④某化学小组设计如下实验方案,证明苯和溴发生的是取代反应而不是加成反应。
第一步:取少量反应后F装置中的溶液于试管中;第二步:向其中加入过量的稀硝酸;第三步:继续滴加少量的硝酸银溶液。如果有浅黄色沉淀生成则证明苯和溴发生的是取代反应。
该实验方案________(填“合理”或“不合理”),理由是___________________________。
在常温下,下列五种溶液:
①0.1mol/L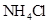 ②0.1mol/L
②0.1mol/L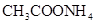 ③0.1mol/L
③0.1mol/L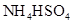
④0.1mol/L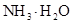 和0.1mol/L
和0.1mol/L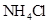 混合液⑤0.1mol/L
混合液⑤0.1mol/L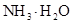
请根据要求填写下列空白:
(1)溶液①呈性(填“酸”、“碱”或“中”),其原因是(用离子方程式表示)
____________________________________________________________________________。
(2)在上述五种溶液中,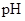 最小的是;
最小的是; 最小的是(填序号)
最小的是(填序号)
(3)比较溶液②、③中 的大小关系是②③(填“>”、“<”或“=”)。
的大小关系是②③(填“>”、“<”或“=”)。
(4)在溶液④中,离子的浓度为0.1mol/L;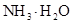 和离子的物质的量浓度之和为0.2mol/L。
和离子的物质的量浓度之和为0.2mol/L。
(5)常温下,测得溶液②的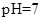 ,则说明
,则说明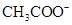 的水解程度(填“>”、“<”或“="”" )
的水解程度(填“>”、“<”或“="”" )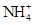 的水解程度,
的水解程度,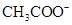 与
与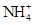 浓度的大小关系是:
浓度的大小关系是: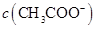
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
下表是周期表的一部分,试回答下列问题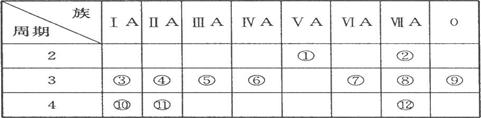
(1)、表中元素中,第一电离能最小的元素是(填元素符号,下同),电负性最大的元素是,单质中化学性质最不活泼的是__________ (填化学式)。
(2)、表中元素的最高价氧化物对应水化物中,酸性最强的是(填化学式,下同),碱性最强的是,呈两性的氢氧化物是。
(3)、表中ⅦA元素中最不稳定的氢化物是__________(填化学式)。
(4)、为什么表中的④第一电离能比⑤大?
______________________________________________。
弱电解质的电离平衡、盐类的水解平衡和难溶物的沉淀溶解平衡均属于化学平衡。
I、已知H2A在水中存在以下平衡:H2A H++HA-,HA-
H++HA-,HA- H++A2-。
H++A2-。
⑴Na2A溶液显碱性的原因(用离子方程式回答)。
⑵某温度下,若向0.1 mol/L的NaHA溶液中逐滴滴加0.1 mol/L KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是。
A.c(H+)·c(OH-)=1×10―14B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)D.c(Na+)+c(K+)=0.05 mol/L
⑶已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:
CaA(s) Ca2+(aq)+A2-(aq)△H>0。
Ca2+(aq)+A2-(aq)△H>0。
①降低温度时,Ksp(填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+)。
II、⑷已知常温下Mg(OH)2在pH=12的NaOH溶液中Mg2+的浓度为1.8×10-7mol/L,则 Ksp[Mg(OH)2]=。
X、Y、Z三种元素,原子序数依次减小。X是第四周期主族元素,其部分电离能如图17所示;X、Y元素具有相同的最高正化合价;Z元素是形成化合物种类最多的元素。回答下列问题: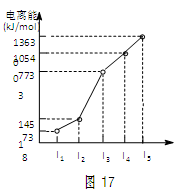
(1)已知Y元素的电负性为1.2,氮元素的电负性为3.0,则Y与氮形成的化合物的化学式为,该化合物的晶体类型为
(2)电负性:X ______Y(填“>”、“=”或“<”)。
(3)元素Z的一种氢化物(化学式为Z2H4)是重要的化工原料。有关Z2H4分子的说法正确的是__________(填字母)。
| A.分子中含有氢键 |
| B.分子中既含有极性键又含有非极性键 |
| C.含有4个σ键和1个π键 |
| D.属于非极性分子 |
(4)X的氧化物与钛(Ti)的氧化物相互作用,能形成钛酸盐,其晶体结构示意图如图18所示(X、Ti和O三种元素对应的离子分别位于立方体的体心、顶点和面心)。该晶体中,钛离子和周围________(填数字)个氧离子相紧邻。
(5)X的氧化物的熔点比Y的氧化物的熔点(填“高”或“低”),
原因是。
X、Y、Z、W、Q 五种元素原子序数依次增大,X原子核外的L层电子数是K层的两倍,Z原子外围电子排布式为nsnnp2n,W原子核外的M层中只有两对成对电子,Q的核电荷数是Z与W的核电荷数之和。请回答下列问题:
(1)X、W的元素符号依次为、;
(2)写出Y2的电子式____________________;
(3)WZ2与XZ2分子的空间结构分别是和,相同条件下两者在水中的溶解度较大的是(写分子式);
(4)Q在元素周期表区(填s、p、d、ds、f),其外围电子排布式为,在形成化合物时它的最高化合价为。