黄铜矿(主要万分
)经初步处理后,所得溶液甲中的溶质为
、
及
。某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如图所示:

(1)
与铁反应的化学方程式:
,其中
为化学计量数,
的值为。
(2)步骤Ⅰ中,生成铜的化学方程式:。
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是。
(4)步骤Ⅱ中加入一种可溶性可实现其转化,从复分解反应发生的条件分析,该试剂可以是。
(5)步骤Ⅲ回收铜的方法为。
通过观察和实验的方法可获知物质的性质,从物质的状态、颜色、温度变化、有无沉淀或气体生成等方面可寻找物质发生变化的证据,分析各种证据能加深对物质变化和变化规律的认识。请回答:
(1)将锌粒放入稀硫酸中,锌粒表面产生气泡,产生该气泡的化学方程式为 ;
(2)经引燃的铁丝在氧气中燃烧,支持铁和氧气发生化学反应的最主要证据是 。
化学反应的过程就是组成反应物分子的原子重新组合成生成物分子的过程。如图是处理汽车排放的某种有毒气体的微观模型。请回答:

(1)用模型表示方框中的微粒 ;
(2)该反应属于基本化学反应类型中的 。
某兴趣小组对氢氧化钡溶液和稀盐酸混合后是否发生了化学反应展开了系列实验。
【实验操作】
用试管取6毫升氢氧化钡溶液,往试管中加入6毫升稀盐酸,等分成两份。
【实验证明】
(1)往其中一份混合液中滴入几滴酚酞试液,发现溶液呈无色。说明溶液中不存在的离子是 ,证明两者发生了反应。
【继续探究】
(2)能否再设计一个实验证明盐酸中H+参加了反应?于是往混合液中滴入石蕊试液,发现变红色,溶液呈酸性,这不能证明盐酸中H+参加了反应。讨论后,形成了新的对照实验方案,将步骤补充完整:
①往盛有另一份混合液的试管中,加入足量的镁片;
② ,加入等量的镁片。
(3)证明原混合液的盐酸中H+参加了反应的现象是 。
【微观解释】
(4)从微观上分析:氢氧化钡溶液和稀盐酸反应的实质是 。

某兴趣小组在实验室相对封闭的装置内燃烧某种含碳、氢、氧元素的垃圾,对产生的废气成分(不考虑气态有机物)按如图所示的装置进行检验。
【实验研究】
拉动注射器,让废气依次通过装置。

【实验分析】
(1)能证明废气中有水蒸气存在的现象是 ;
(2)F处的大号注射器,可以引导气体流向,其另一个主要作用是 ;
【反思评价】
(3)小金认为,仅根据E中澄清石灰水变浑浊,无法确定一氧化碳的存在,其理由是 ;
(4)小金根据D中的粉末由黑色变为红色,得出废气中存在一氧化碳。小丽认为该结论不够严密,若废气中存在氢气也会出现该现象。要使上述结论更加严密,还应添加的一个实验装置及位置是 。
【实验结果】
经检验,废气中存在CO2、CO、H2O。
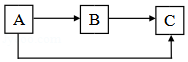
A、B、C为初中科学常见的三种无机物,它们之间有如图所示的转化关系(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去)。请回答:
(1)若C是气体,它能使带火星的木条复燃,A、B所属的物质类别和组成元素都相同,则A→B的化学方程式为 ;
(2)若A为光合作用的原料之一,A与B属于不同物质类别,B和C属于同种物质类别,A、B、C三种物质中都含有相同的两种元素,则C可能的物质类别是 。