焦炭是工业生产中的重要还原剂和燃料,活性炭用于生活和实验室中通过吸附作用除去有害气体或有毒物质。它们的化学成分都可以看成是碳单质。
(1)红热的焦炭投入浓硝酸中,写出反应的化学方程式 ;
(2)将一定条件下的高锰酸钾溶液与活性炭混合,可发生如下反应(未配平)
MnO4-+ C+ H2O—— MnO2+ ① +CO32-
则 ① 处应该填入的微粒化学式为 ;
(3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。
写出反应管a中发生的所有反应的化学方程式 。
(7分)已知(1)丙烯与水进行加成反应,其可能的产物有两种:(2)下图中E为开链的酯类化合物,其分子式为C6H12O2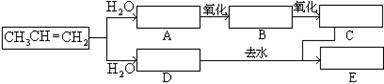
(1)请依据上述条件和图中转化关系,在方框中填入合适的化合物的结构简式。
(2)B和银氨溶液反应生成C的化学方程式。
(7分)从某些植物树叶中提取的有机物中含有下列主要成分:
(1)写出C的分子式________。
(2)用A、B、C、D填空:
①能 发生银镜反应的有________;②既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的有___________。
发生银镜反应的有________;②既能使FeCl3溶液显紫色又能和NaHCO3反应放出气体的有___________。
(3)写出C同时满足下列条件的一种同分异构体:①含苯环且环上有两个取代基;②取代基没有环状结构;③遇FeCl3溶液发生显色反应:
(4 )写出D与乙醇反应生成酯的化学反应方程式。
)写出D与乙醇反应生成酯的化学反应方程式。
(6分)下面给出了四种烃A、B、C、D的相关信息:
①烃A在所有的烃中含碳的质量分数最低
②烃B是一种植物生长调节剂,可用于催熟果实
③烃C在氧气中燃烧产生的氧炔焰常用来切割或焊接金属
④烃D的分子比例模型如图所示:
据此回答有关问题:
(1)将A和Cl2混合充入一试管,密封后置于光亮处,一段时间后能看到试管内壁上出现的油状物不可能是(填编号)
A.CH3Cl B. CH2Cl2C. CHCl3 D CCl4
CCl4
(2)写出实验室制取B的反应类型。
(3)实验室制取C的化学方程式为。
(4) D分子中不存在碳碳单键和碳碳双键交替结构,以下能证实这一事实的是。
a.D的邻位二氯取代物不存在同分异构体
b.D的间位二氯取代物不存在同分异构体
c.D的对位二氯取代物不存在同分异构体
(5)某有机化合物X的相对分子质量大于70,小于120。经分析得知,其中碳元素和氢元素的质量分数之和为68%,其余为氧元素。则X的分子式为 。
。
(4分)写出下列各化学用语
-CH2CH3(名称),-NO2(名称),-OH(电子式),羧基(化学符号)
与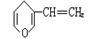 互为同分异构体的酚类化合物的同分异构体最多有
互为同分异构体的酚类化合物的同分异构体最多有
| A.3种 | B.4种 | C.5种 | D.6种 |