由2氯丙烷制取少量的1,2丙二醇 时,需要经过的反应是
时,需要经过的反应是
| A.加成→消去→取代 | B.消去→加成→水解 |
| C.取代→消去→加成 | D.消去→加成→消去 |
有一化学平衡:mA(g)+nB(g) pC(g)+qD(g)(如右图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是( )
pC(g)+qD(g)(如右图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是( )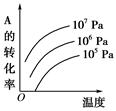
| A.正反应吸热:m+n>p+q | B.正反应吸热:m+n<p+q |
| C.正反应放热:m+n>p+q | D.正反应放热:m+n<p+q |
可逆反应mA(g) nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )
nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )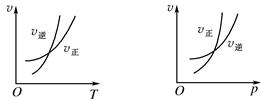
| A.m>n,Q>0 | B.m>n+p,Q>0 | C.m>n,Q<0 | D.m<n+p,Q<0 |
在一定温度下将1 mol CO和1 mol水蒸气放入一固定容积的密闭容器中,反应CO(g)+H2O(g) CO2(g)+H2(g)达平衡后,得到0.6 mol CO2;再通入0.3 mol水蒸气,达到新平衡状态后,CO2的物质的量可能是( )
CO2(g)+H2(g)达平衡后,得到0.6 mol CO2;再通入0.3 mol水蒸气,达到新平衡状态后,CO2的物质的量可能是( )
| A.0.9 mol | B.0.8 mol | C.0.7 mol | D.0.6 mol |
某温度下,将2 mol A和3 mol B充入一密闭的容器中发生反应:aA(g)+B(g) C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为
C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为
| A.40% | B.60% | C.24% | D.4% |
下列离子方程式中,书写正确的是
| A.铁片投入到稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| B.氧化镁与稀盐酸混合:MgO+2H+=Mg2++H2O |
| C.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D.稀盐酸滴在石灰石上:CO32-+2H+=H2O+CO2↑ |