用(相同的物质、同素异形体、同系物、同分异构体、同位素)填空
(1)2-甲基丁烷和丁烷 ________________。
(2)正戊烷和2,2-二甲基丙烷___________________。
(3)间二甲苯和乙苯_____________________ 。
(4)1-已烯和环已烷_________________。
(5)白磷和红磷____________________。
(1)阿波罗宇宙飞船使用的是以KOH为介质的氢、氧燃料电池(如下图),按下列要求填空: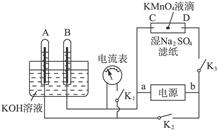
(1)①__________(填“负”或“阴”)极反应式:;②__________(填“正”或“阳”)极反应式:_________________;③电池反应式_________________________________。
(2)如图所示装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹;电源有a、b两极。若A、B中充满KOH溶液后倒立于KOH溶液的水槽中,切断K1,闭合K2、K3通直流电,回答下列问题:
①判断电源的正、负极:a为___________极,b为极___________。
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象?______________________。
③写出电极反应式:A极______________________,C极______________________。
④若A极产生气体的体积在标准状况下为x L,则C极上产物的质量大约为___________g。
⑤若电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针是否移动___________(填“是”或“否”)。若电流表指针不移动说明理由,若指针移动也说明理由。
如下图所示,若电解5 min铜电极质量增加2.16 g。试回答: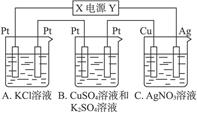
(1)电极X是电源的___________极。
(2)pH变化:A___________;B___________;C___________。
(3)若A中KCl溶液的体积为200 mL,电解至5 min溶液的pH是__________(假设溶液体积不变化)。
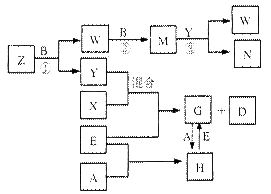 A、B、C、D、E是中学化学常见的五种单质,已知A、B、C、D在常温下均为气态,E为金属,其中D能分别跟A、B、C在一定条件下化合,生成对应的化合物X、Y、Z,其中常温下,Y为液体,X、Z为气体。有关的转化关系如下图所示(反应条件均已略去)。
A、B、C、D、E是中学化学常见的五种单质,已知A、B、C、D在常温下均为气态,E为金属,其中D能分别跟A、B、C在一定条件下化合,生成对应的化合物X、Y、Z,其中常温下,Y为液体,X、Z为气体。有关的转化关系如下图所示(反应条件均已略去)。
(1)化合物Z的空间构型为;构成A的元素的最高价氧化物水化物的化学式为;实验室贮存N的方法是。
(2)写出反应②的化学反应方程式;G→H的离子方程式。
(3)常温下,D与A反应生成1 mol X时放热92.3kJ,写出该反应的热化学方程式:
。
(4)将过量的E加入N的稀溶液中,若反应过程中转移电子的数目为3.01×1023,则参加反应的E的质量为g。
已知:G是一种常用的药用有机物,合成路线如图所示:
①有机物A和C都能与FeCl3发生显色反应,且取代基处于邻位
②有机物G只含碳、氢、氧元素且式量小于200,氧元素的质量分数为35.56%。
请回答:
(1)写出A、C、K的结构简式A________C________K__________
(2)反应①~⑨中,属于取代反应的有______________(填序号)
(3)写出F的常见同分异构体与F在浓硫酸条件下的反应_____________________
(4)写出G在加热条件下与NaOH溶液反应的化学方程式_______________________
(5)写出反应⑥的方程式____________________。
萝卜中具有较多的胡萝卜素,它是人体的主要营养之一。α-胡萝卜素的结构为: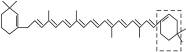
(1)写出α-胡萝卜素的分子式________。
(2)1 mol胡萝卜素最多能与________ mol Br2反应。
(3)β-胡萝卜素与α-胡萝卜素互为同分异构体,且只是虚线框内部分不同,但碳的骨架相同,写出β-胡萝卜素方框内可能的结构简式:______________________。