下列叙述正确的是
①配位键在形成时,是由成键双方各提供一个电子形成共用电子对
②C60晶体的晶胞是面心立方结构
③Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]4s24p2,属于P区元素
④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子
⑤冰中存在极性共价键和氢键两种化学键的作用
⑥Cu(OH)2是一种蓝色的沉淀,既溶于硝酸、浓硫酸,也能溶于氨水中
⑦熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体
⑧氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为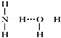
| A.②⑥ | B.②③ | C.⑤⑥ | D.③⑥ |
下列有关电负性的说法中正确的是( )
| A.主族元素的电负性越大,元素原子的第一电离能一定越大 |
| B.在元素周期表中,元素电负性从左到右越来越大 |
| C.金属元素电负性一定小于非金 属元素电负性 |
| D.在形成化合物时,电负性越小的元素越容易显示正价 |
一基态原子的第五电子层只有2个电子,则该原子的第四电子层上的电子数可能为( )。
| A.8 | B.18 | C.8~18 | D.18~32 |
下列电子排布式对应的元素原子,半径最大的是 ()。
| A.1s22s22p63s23p64s1 | B.1s22s22p63s23p63d104s1 |
| C.1s22s22p63s23p63d104s24p5 | D.1s22s22p63s23p 63d54s2 |
下列说法不正确的是()
| A.同族元素,随着核外电子层数的增加,I1逐渐增大 |
| B.通常情况下,对于同一种元素的原子,其电离能I1<I2<I3 |
| C.同周期元素,总体变化趋势是随着核电荷数的增加,I1增大 |
| D.通常情况下,电离 能越小,元素的金属性越强 |
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于四 种元素的描述,不正确的是()
| A.原子半径:X>Y>W>Z | B.原子序数 :Y>X>Z>W |
| C.原子最外层电子数:Y>X>Z>W | D.金属性:X>Y,还原性:W2->Z- |