乙烯是重要的有机化工原料。
(1)实验室中,乙烯可由乙醇脱水制得。工业上,乙烯的获取主要来自于石油的 。
(2)将乙烯通入溴水中,可以观察到溴水褪色,请写出反应的化学方程式并注明反应类型: ,反应类型为 。
(3)下列物质与乙烯催化加氢得到的产物互为同系物的是 (选填编号)。
a.C2H6 b.C3H6 c.C3H8 d.C4H8
(4)水果保鲜时常使用浸泡过高锰酸钾溶液的硅藻土,其原因是 。
已知X和Y各是由两种常见元素组成的化合物,A.B为气体,G为白色沉淀,F是一种两性氢氧化物,在电解开始时,溶液中有白色沉淀产生,但随着电解的进行,白色沉淀逐渐溶解,最后变为澄清溶液C(有两种溶质),X.W.C.E的焰色反应均为黄色。各物质之间的关系如图所示(部分产物已经省略,除气体间的反应外,其余反应均在溶液中进行)。
(1)X、Y、W的化学式分别为..
(2)写出反应①的离子方程式
(3)A与B反应生成1 mol D时放出热量为92.3 kJ,则此反应的热化学方程式为。
(4)向澄清溶液C中加入10 mol·L-1的硫酸,当加至50 mL时才开始出现沉淀,假设电解过程中溶液体积变化忽略不计,原X和Y混合液的体积为100 mL,Y溶液的物质的量浓度为a mol·L-1,则X溶液的物质的量浓度为mol·L-1(含a代数式表示)。
常温下,10ml某烃A和80ml O2(过量)混合,点燃使其充分燃烧后恢复到原始状态,残留气体体积为65ml。
(1)若A为烷烃,则其分子式为
(2)若A为烯烃,则其分子式为
(3)若A为炔烃,则其分子式为
(4)若A为本或苯的同系物,则其分子式为
有机化学反应因反应条件不同,可生成不同的有机产品。例如:
(1)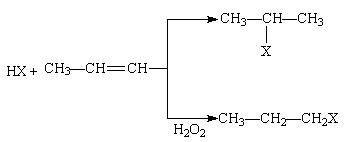 (X为卤素原子)
(X为卤素原子)
(2)苯的同系物与卤素单质混合,若在光照条件下,侧链上氢原子被卤素原子取代;若在催化剂作用下,苯环上的氢原子被卤素原子取代。
工业上利用上述信息,按下列路线合成结构简式为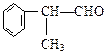 的物质,该物质是一种香料。
的物质,该物质是一种香料。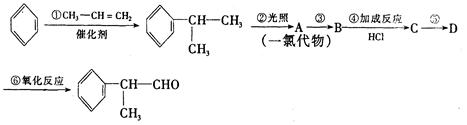
请根据上述路线,回答下列问题:
(1)A的结构简式可能为____________________________________。
(2)反应①、③、⑤的反应类型分别为________、________、_______。
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件):
______________________________________________。
(4)这种香料具有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色②分子中有苯环,且苯环上的一溴代物有两种。写出符合上述条件的物质可能的结构简式(只写两种):
____________________________________________________________。
已知:①R— —
—
②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
以下是用苯作原料制备一系列化合物的转化关系图:
(1)A转化为B的化学方程式是_______________________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①、②物质的结构简式:
①________________________,②____________________________。
(3)B在苯环上的二氯代物有种同分异构体。
(4)有机物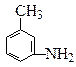 的所有原子(填“在”或“不在”)同一平面上。
的所有原子(填“在”或“不在”)同一平面上。
正盐A能发生下图所示的反应,图中①~⑧分别代表有关反应中的一种物质(某些物质已略去),其中①、②、④、⑤为无色气体。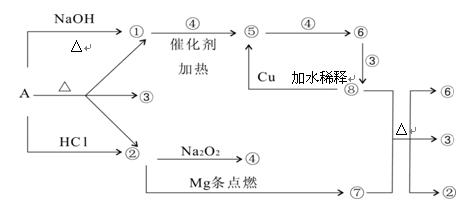
请完成下列各题:
(1)写出化学式A ⑥ ⑦
(2)写出下列反应方程式:
⑧+⑦ ②+③+⑥:
②+③+⑥:
①+④ ⑤:
⑤:
(3)⑧ ⑤的离子方程式为:
⑤的离子方程式为: