溶液能对过氧化氢的分解起催化作用,某小组拟在相同浓度
溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
写出本实验发生反应的化学方程式
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的
溶液,如图观察到
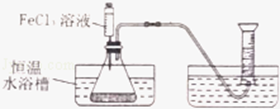
为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设计.
Ⅱ.
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
[方案二]在不同过氧化氢浓度下,测定
方案二的实验测量结果:
 |
30%
溶液的体积(mL) |
2%
溶液的体积(mL) |
加入
的体积(mL) |
反应的时间(min) |
生成
的体积(mL) |
| 1 |
5 |
x |
20 |
5 |
V1 |
| 2 |
10 |
3 |
15 |
y |
V2 |
表中
=
实验结论:通过测量,若V1
【改编】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
(1)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是________。
(2)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 |
FeO |
Fe2O3 |
Fe3O4 |
| 颜色、状态 |
黑色粉末 |
红棕色粉末 |
黑色晶体 |
| 能否被磁铁吸引 |
否 |
否 |
能 |
Fe3O4+8HCl= FeCl2+2FeCl3+4H2O
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引,那么该黑色固体不可能含有_______(化学式),
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________。
【实验探究】
| 实验操作 |
实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为___________________________________。
【反思与交流】初中我们还学过通过_______________________________(化学方程式)得到Fe3O4。
【改编】铜制器物在潮湿环境中表面会产生绿色的锈迹,俗称铜绿。某化学学习小组对铜绿成分产生了浓厚兴趣。
【提出问题】铜绿中除铜元素外还有其它什么元素?
【查阅资料】①无水硫酸铜遇水变蓝色;②碳与一般的酸不反应;
【实验探究】该小组同学找到了一些铜绿粉末并进行了如下实验:
【观察分析】A装置中绿色粉末变为黑色;B装置中无水硫酸铜变为蓝色;
C装置中澄清石灰水变浑浊,该反应的化学方程式为 。
【实验结论】铜绿中除铜元素外还有 和碳等元素。
【交流讨论】根据铜绿的组成,小组同学对A装置中产生的黑色粉末的成分有如下两种不同的猜想:
(1)全部为CuO
(2)全部为C
(3)CuO和C的混合物
【深入探究】
| 实验步骤 |
实验现象 |
实验结论 |
| ①取少量黑色粉末于试管中,滴加足量的稀硫酸 |
①固体全部溶解,溶液颜色变蓝 |
猜想(1)正确 |
| ②取少量黑色粉末于试管中,滴加足量的稀硫酸 |
② |
猜想(2)正确 |
| ③取少量黑色粉末于试管中,滴加足量的稀硫酸 |
③(2分) |
猜想(3)正确 |
【实验结论】化学学习小组同学通过实验证明猜想(1)正确。
【反思应用】根据铜绿中所含元素,可知铜生锈不仅与空气中的氧气、水有关,还可能与空气中的 等有关;要保护博物馆里的青铜器,减缓生锈,我们可以减少青铜器与 接触。
【改编】竹子是“有节、中空、四季常绿”的植物。同学们对竹子中的气体成分展开了探究,测定其成分。
【查阅资料】①莲藕也有类似空腔,以贮备空气帮助呼吸作用;②红磷的着火点为240 ℃,白磷的着火点为40 ℃。
【猜想】①竹子中气体成分也和空气一样,含有氧气、氮气和二氧化碳;②氧气含量比空气的更少
【进行实验】
(1)收集竹子中的气体。
A组:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体。
B组:可用注射器从竹子中抽取气体。
(2)检验气体中是否含有二氧化碳气体(氧气、氮气略)。
| 实验方法 |
实验现象 |
实验结论 |
| 向所取气体中加入过量的澄清石灰水 |
|
竹子中气体含有二氧化碳 |
(3)测定氧气含量。
如下图所示的方案一和方案二来测定氧气含量。
【反思与评价】
a.两个方案的实验测定结果不同,测定结果比较准确的是方案 ,原因是 。
b.两个方案进入的水都约占总体积的1/7左右,那么竹子气体含有的氧气含量 (大于、等于、小于)空气中氧气含量;
c.经过A、B两组同学的实验,A组测得的竹子中含氧量总是大于B组的,你认为原因是 。
【改编】化学兴趣小组以酸、碱、盐的性质为主题,进行探究学习,请完成下列问题.
(1)初中常见的酸有四种,既有各自的特点:如汽水中含有碳酸以增加口感;浓硝酸遇光、热易分解,因此保存时要 ;浓盐酸打开瓶盖后会形成白雾,是因为 ;浓硫酸溶于水时会放出极多的热,因此稀释时应 (操作方法);但酸也都具有相似的性质,因为 。
(2)小组同学将无色酚酞溶液分别滴入NaOH溶液、Ca(OH)2溶液中,溶液均由无色变为 色.通入二氧化碳,都能发生反应中和碱性,写出其中发生一个有沉淀生成的中和反应 (化学方程式,2分).NaOH 和Ca(OH)2若密封保存不当很容易变质,可以通过 (实验方法和现象,2分)来检测是否变质;
(3)将Ca(OH)2溶液与Na2CO3溶液反应后所得混合物进行过滤,向滤液中滴入几滴稀盐酸,无明显现象,则原滤液中溶质的组成可能是 .
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
将气体通入澄清的石灰水中 |
澄清石灰水变浑浊 |
| ② |
将带火星的木条伸入该气体中 |
带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________,写出该反应的化学方程式_____________________________________________________。
(2)由实验② (填“能”或“不能”)确定该气体中不含氧气。
探究二:维C泡腾片溶液的酸碱性。
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显 性。