实验室常用下列装置制取气体,请你根据所学知识回答下列问题。

(1)仪器a的名称是 。
(2)实验室制取氧气时,选用的收集装置是 (填字母序号)。
若改用下图装置收集氧气,则气体应从 进(填“a”或“b”)。

(3)小明取一定浓度的盐酸与石灰石反应制取气体,反应的化学方程式为______________________________;将生成的气体通入澄清石灰水中,未见变浑浊。为探究其原因,进行了如下过程:
【作出猜想】A.石灰水已经完全变质; B.气体中有挥发出来的HCl气体。
【实验探究】
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色。于是排除了猜想A,你认为排除猜想A的理由是_____________。
②小明想探究所得气体中是否有挥发出来的HCl气体,设计如下实验。请你帮他完成实验,填写以下表格:
| 实验步骤 |
实验现象 |
实验结论 |
| |
|
气体中有HCl |
【查阅资料】
碳酸钠溶液中通入二氧化碳发生反应: Na2CO3 + CO2 + H2O = 2NaHCO3
【拓展延伸】
如果用上述原料制得纯净的二氧化碳气体,所选仪器的连接顺序为 (填字母)。
MnO2是重要无机材料,某学习小组设计了将粗MnO2(含有较多的MnO、 MnCO3和Fe2O3,其中Fe2O3质量百分含量为10%)样品转化为纯MnO2实验,其流程如下:
(已知:氧化性强弱顺序: ClO3-> MnO2 > Fe3+)
(1)铝与二氧化锰在高温下发生铝热反应,相关反应的化学方程式为:。
(2)第②步反应离子方程式为:。
(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、玻璃棒、、;
第③步蒸发得到的固体中除了含有NaClO3和NaOH外,还一定含有(写化学式)。
(4)MnO2是碱性锌锰电池的正极材料,则碱性锌锰电池放电时,正极的电极反应式是:。
(5)若粗MnO2样品的质量为28.2g,第①步反应后,经过滤得到17.4g MnO2,并收集到448mL CO2(标准状况下),则在第②步反应中至少需要mol NaClO3才能将Mn2+完全转化为MnO2。
某课外小组探究钠、铝、铁、铜单质还原性强弱及其相关化学性质,做了如下实验:
| 实验1 |
常温时取四种金属少量分别放入装有蒸馏水的试管中 |
| 实验2 |
再取少量铝、铁、铜分别放入装有稀硫酸的试管中 |
(1)实验1中能发生反应的离子方程式。
(2)实验2中能够判断出铝、铁、铜还原性强弱的现象是。
结论:由实验1、2得出四种金属的还原性强弱顺序为;请从原子结构角度解释钠的还原性强于铝。
(3)为确认实验2反应后溶液中的金属阳离子,再进行实验:
①取Al反应后的溶液加入过量的NaOH溶液,写出反应的离子方程式。
②一段时间后,取Fe反应后的溶液,检验Fe2+方法正确的是。
a.滴加KSCN溶液,无明显变化,再加入少量氯水,溶液变红
b.滴加K3[Fe(CN)6]溶液,有蓝色沉淀产生
c.滴加NaOH溶液,产生的白色沉淀迅速变成灰绿色,最终变成红褐色
(4)在实验2中,铝、铁反应现象的差异并不是很明显,有同学建议再设计一种实验来证明这两种金属的还原性关系,请设计一种实验方案。
(5)在实验过程中,还有同学为了验证铁与铜的还原性,用铁、铜、导线、烧杯、氯化铁溶液设计了原电池装置。
①画出原电池的装置图。
②该电池的正极反应为。
根据要求完成下列各题实验目的.(a、b为弹簧夹,加热及固定装置已略去)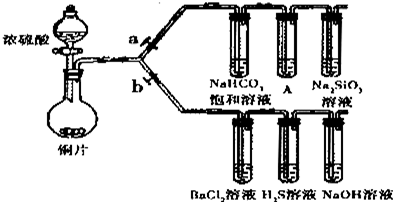
(1)验证碳、硅非金属性的相对强弱.
①实验操作:连接仪器、______、加入药品,打开a关闭b,滴入浓硫酸,加热.
②铜与浓硫酸反应发生的化学方程式是______.
③能说明碳的非金属性比硅强的实验现象是:______.
(2)验证 SO2的氧化性、还原性和酸性氧化物的通性.
①打开b,关闭a.能验证SO2具有氧化性的化学方程式是______.
②若大量二氧化硫通入氢氧化钠溶液中,化学方程式________________________
③BaCl2溶液中无沉淀现象,将其分成两份,分别低价下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 |
氯水 |
氨水 |
| 沉淀的化学式 |
某化学兴趣小组用下图所示装置来制取二氧化硫并探究其性质:
请回答下列问题:
(1)A中发生反应的化学方程式是________________________。
(2)实验过程中,B试管内发生的现象是,SO2与过氧化钠的漂白原理不同之处在于。
(3)设计装置C是为了证明SO2的性,实验现象是。
(4)设计装置D是为了证明SO2的性,反应的化学方程式是。
(5)仪器a的名称是,其作用是。
(6)若将E的烧杯中溶液换为漂白粉溶液,实验过程中会产生白色沉淀,该沉淀的化学式是。
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A、滴定管内液面的变化
B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是由此造成的测定结果(偏高、偏低或无影响)
(4)步骤②缺少的操作是
(5)下图,是某次滴定时的滴定管中的液面,其读数为 mL
(6)根据下列数据:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
4.00 |
24.10 |
请计算待测烧碱溶液的浓度(保留四位小数)mol/L