水是生命之源,也是化学反应中的主角。请回答下列问题:
Ⅰ、氢气燃烧生成液态水热化学方程式是2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ/mol。
(1)生成物能量总和 (填“大于”、“小于”或“等于”)反应物能量总和。
(2)若2 mol氢气完全燃烧生成水蒸气,则放出的热量 572 kJ(填“>”、“<”或“=”)。
(3)氢气热值为 。
Ⅱ、氢气和氧气反应生成水,将化学能转化为电能,其构造如图所示:a、b两个电极均由多孔的碳块组成。
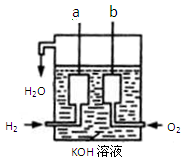
(1)a电极反应式是 。
(2)b电极反应式是 。
Ⅲ、如图表示一个电解池。X、Y都是惰性电极,电解液a是饱和食盐水,同时在两边各滴入几滴酚酞试液。
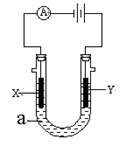
(1)X极上的电极反应式为 ,在X极附近观察到的现象是 。
(2)Y极上的电极反应式为 ,检验该电极反应产物的方法是 。
某小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol·L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
(1)滴定前是否要滴加指示剂?(填“是”或“否”),请说明理由。
(2)滴定时用(填a或b)滴定管盛装KMnO4标准溶液。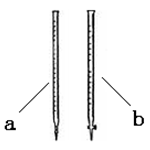
(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为。
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:
⑴按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
A接,接,接。
⑵仪器乙、丙应有怎样的实验现象才表明已检验出CO2?
乙中,
丙中。
⑶丁中酸性KMnO4溶液的作用是;
⑷写出甲中反应的化学方程式。
制取氨气并完成喷泉实验(图中夹持装置均已略去)
⑴写出实验室制取氨气的化学反应方程式:
⑵收集氨气应使用法,要得到干燥的氨气可选用做干燥剂。
⑶收集氨气时,验满的方法是。
⑷用下图装置进行喷泉实验,上部烧瓶已装满干燥氨气,引发水上喷的操是,该实验的原理是。
⑸假设烧瓶充满标况下的氨气,喷泉实验后溶液充满整个烧瓶,所得溶液物质的量浓度为。
某实验小组用工业上废弃固体(主要成分Cu2S和Fe2O3)混合物制取粗铜和Fe2(SO4)3晶体,设计的操作流程如下:
(1)除酒精灯和铁架台或三脚架外,①中所需的容器和夹持仪器分别为、
,①和⑥中都用到的仪器为;
(2)试剂x的化学式为;x与溶液B反应的离子方程式为;
(3)某同学取少量的溶液B向其中加入过量的某种强氧化剂,再滴加KSCN溶液,发现溶液变红色,放置一段时间后,溶液褪色,该同学猜测溶液褪色的原因是溶液中的SCN-被过量的氧化剂氧化所致。
现给出以下试剂:1.0 mol·L-1 硫酸、1.0 mol·L-1 NaOH溶液、0.1 mol·L-1 Fe2(SO4)3溶液、20%KSCN溶液、蒸馏水。请你设计合理实验验证乙同学的猜测是否合理。简要说明实验步骤和现象;
(4)某同学用实验制得的Fe2(SO4)3晶体配制0.1 mol·L-1的Fe2(SO4)3溶液,在称量出Fe2(SO4)3晶体后,溶解该晶体的具体操作为。
(13分) 下图是实验室中制备气体或验 证气体性质的装置图
证气体性质的装置图
(1)仪器a的名称是_________________。
(2)利用上图装置制备纯净、干燥的氯气。
①圆底烧瓶内发生反应的化学方程式为____________________________________。
②装置B中的溶液为_________________;烧杯中溶液的作用为____________________  。
。
③E装置发生反应的离子方程式为____________________________________。
(3)在上图所示圆底烧瓶内加入碳,a中加入浓硫酸,开始实验,加热产生的气体缓慢通过后续装置完成如下实验:
实验1:证明SO2具有漂白性和还原性
实验2:证明碳元素的非金属性比硅元素的强
①B中为少量品红溶液,C中为少量酸性KMnO4溶液,则证明SO2具有漂白性的现象为__________________________________________。
②D中应加入足量的____________(填溶液名称),E中加入____________(填溶液名称),证明碳元素的非金属性比硅元素的强的现象为___________________________。
③为提高实验2的准确性,必须改进的装置为___________________。(填装置代号)