【2015天津理综化学】(14分)随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。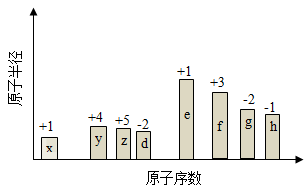
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的小(用化学式表示,下同)_______>__________;比较g、h的最高价氧化物对应的水化物的酸性强弱是:_______>__________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式:___________。
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下: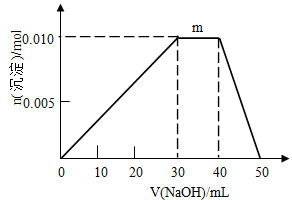
①R离子浓度由大到小的顺序是:__________。
②写出m点反应的离子方程式____________。
③若R溶液改加20mL1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_______mol。
在KI 淀粉溶液中,滴加少量Na2ClO溶液,并加入少量稀H2SO4,溶液立即变蓝,这是因为____________,离子方程式是________________。
在上述蓝色的溶液中滴加足量的Na2SO3溶液,蓝色逐渐消失,这是因为_________,离子方程式是________________________________________。
从以上实验可知, ClO-、I2、 的氧化性由强到弱的顺序是_________________________。
的氧化性由强到弱的顺序是_________________________。
相对原子质量大于10的两种短周期元素X和Y能形成两种二元化合物A和B,已知A分子中X和Y的原子个数比为1∶2,A对氧气的相对密度为2,又知B分子中有一个X元素的原子,B在标准状况下的密度为3.57g/L,试判断:(1)X和Y各为何种元素;(2)A和B的化学式。
(1)淡黄色固体的分子构型________________;
(2)黄绿色固体的分子构型________________;
(3)黄绿色固体在水中的溶解度比淡黄色固体大的原因是:_________________________。