(17分)
A、B、C、D、E是位于前三周期的五种元素,原子序数依次增大,其中B与D为同一主族元素,它们可形成化合物DB2、DB3。在同周期元素中,C的金属性最强,E的非金属性最强。请回答:
(1)E的原子结构示意图为。
(2)A、B形成的原子个数比为1∶1的化合物的电子式为,该化合物与DB2化合生成一种强酸的化学方程式为。
(3)已知在一定条件下1 mol气态DB2完全转化为气态DB3,放出98.3 kJ的热量。该反应的热化学方程式是,工业上进行这一反应的设备是。
(4)用铂做电极电解由C、E形成化合物的饱和溶液时,检验阳极产物的实验方法为;电解一段时间后,将阳极产物和阴极溶液混合,反应的离子方程式是。工业中实际常采用阳离子交换膜电解槽进行电解,若某一电极由碳钢网制成,则该电极为电解槽的 (填“阴”或“阳”)极。
已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,所需溶液的pH分别为6.4、6.4、3.7。现由含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其配制成水溶液,然后按图示步骤进行提纯: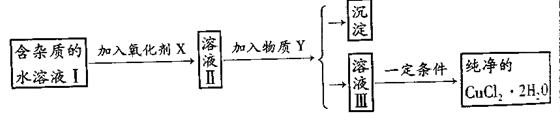
请回答下列问题:
(1)本实验最适合的氧化剂是()(填下面的序号)
| A.K2Cr2O7 | B.NaClO | C.H2O2 | D.KMnO4 |
(2)物质Y是;(用化学式表示)
(3)本实验用碱沉淀法能否达到目的?;原因是;
(4)除去Fe3+的原理是;
经测定某溶液中只含Na+、CH3COO—、H+、OH—四种离子,已知该溶液中含有一种或两种溶质。查资料表明等物质的量浓度的醋酸和醋酸钠等体积混合后溶液呈酸性,试完成下列各题。
(1)试推测能组成这种溶液的可能的溶质或组合是;(用化学式表示)
(2)有关这种溶液,下列说法不正确的是()
A.若溶液中离子间满足c(CH3COO—)>c(Na+)>c(H+)>c(OH—),则溶液中溶质一定为CH3COOH和CH3COONa
B.若溶液中离子间满足c(Na+)>c(CH3COO—)>c(OH—)>c(H+),则溶液中溶质一定只有CH3COONa
C.若溶液中c(Na+)= c(CH3COO—),则该溶液一定呈中性
D.若溶液中c(CH3COOH)>c(Na+),则溶液一定呈酸性
(3)若溶液是由体积相等的醋酸溶液和氢氧化钠溶液混合而成,而且恰好呈中性,则混合前
c(CH3COOH)c(NaOH)(填“大于”、“小于”或“等于”),混合前两溶液中分别的
c(H+)c(OH—)(同上);
(4)若溶液为等体积、等物质的量浓度的醋酸和醋酸钠溶液混合而成,则混合后溶液中的离子浓度关系正确的是。
A.c(CH3COO—) + c(OH—) = c(Na+)+ c(H+)
B.c(CH3COO—)+ 2c(OH—)= c(CH3COOH)+2 c(H+)
C.c(Na+)>c(CH3COO—)>c(H+)>c(OH—)
D.2c(Na+)= c(CH3COOH)+ c(CH3COO—)
完成下列反应的离子方程式:
(1)将AlCl3溶液蒸干得到白色固体:;
(2)用惰性电极电解饱和食盐水:;
(3)用KOH做电解质溶液的甲烷燃料电池的负极反应式:;
(4)往AgCl悬浊液中滴加Na2S溶液:;
从图表中获得有用的信息是化学学习和研究的重要能力。
(1)图1是在一定条件下,反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)的实验曲线。
2CO(g)+2H2(g)的实验曲线。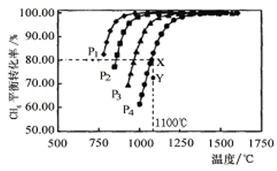
①图中P1、P2、P3、P4代表不同压强,则压强大小的排列顺序为。该反应的△H0(选填“>”、“<”、“=”)。
②压强为 P4时,在 Y 点:υ(正)υ(逆)。(选填“>”、“<”、“=”);
③压强为P4时,密闭容器中CH4和CO2的起始浓度均为0.10mol•L-1,则1100℃时该反应的化学平衡常数
为(保留三位有效数字)。
(2)温度与HCl压强对MgCl2·6H2O受热分解产物的影响如图所示,下列说法正确的是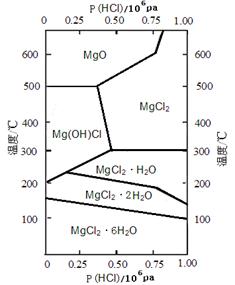
| A.温度低于100℃,MgCl2·6H2O不会发生分解 |
| B.要得到MgO温度至少需要加热至600℃ |
| C.要得到无水MgCl2只要控制温度,不一定要在HCl气体中 |
| D.在HCl气体压强为0.25×106Pa时,温度由室温升高至300℃,发生的反应为MgCl2·6H2O=Mg(OH)Cl+HCl+5H2O |
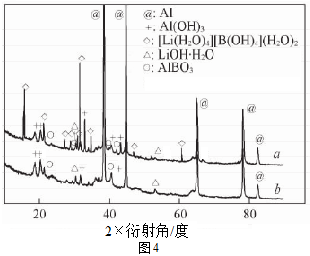
(3)X-射线衍射可用于判断某晶态物质是否存在。Al-LiBH4是新型产氢复合材料,常温下可以与H2O反应生成H2。图3是含LiBH4为25%时Al-LiBH4复合材料的X-射线衍射图谱,图4是该复合材料在25℃(图谱a)和75℃(图谱b)时与水反应后残留固体物质的X-射线衍射图谱。据图分析,25℃时Al-LiBH4复合材料中与水完全反应的物质是__(填化学式),25℃和75℃时产物中不相同的物质是__ (填化学式)。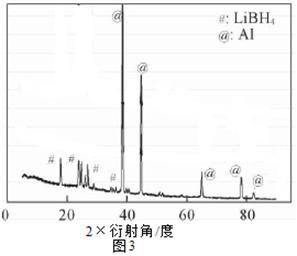
铬铁矿主要成分为FeO·Cr2O3,含有SiO2、Al2O3等杂质。工业上用铬铁矿制备红矾钠(Na2Cr2O7)的流程如下图所示: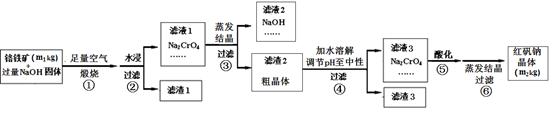
煅烧时反应为:4 FeO·Cr2O3+7 O2 +20 NaOH 8 Na2CrO4 + 4 NaFeO2+10 H2O
8 Na2CrO4 + 4 NaFeO2+10 H2O
(1)步骤①是在坩埚中进行煅烧,可用作此坩埚材料的是。
| A.铁 | B.氧化铝 | C.石英 | D.陶瓷 |
(2)步骤①煅烧反应极慢,需要升温至NaOH呈熔融状态,反应速率才加快,其原因为______。
(3)步骤②中NaFeO2会强烈水解生成氢氧化铁沉淀,其化学方程式为。
(4)将五份滤液1分别在130℃蒸发1小时,各自冷却到不同温度下结晶,保温过滤,所得实验数据如下表。根据数据分析,步骤③的最佳结晶温度为___________。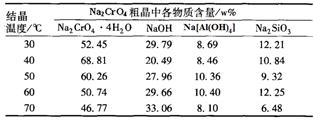
(5)步骤④中滤渣3的成分是_________________________。
(6)假设该流程中铬元素完全转化为红矾钠,则该铬铁矿中铬元素的质量分数为_____(用含m1、m2的代数式表示)。