苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:

相关化合物的物理常数:
| 物质 |
相对分子质量 |
密度(g/cm-3) |
沸点/℃ |
| 异丙苯 |
120 |
0.8640 |
153 |
| 丙酮 |
58 |
0.7898 |
56.5 |
| 苯酚 |
94 |
1.0722 |
182 |
回答下列问题:
(1)在反应器A中通入的X是 。
(2)反应①和②分别在装置 和 中进行(填装置符号)。
(3)在分解釜C中加入的Y为少量浓硫酸,其作用是_____,优点是用量少,缺点是__________。
(4)反应②为_____(填“放热”或“吸热”)反应。反应温度控制在50-60℃,温度过高的安全隐患是 。
(5)中和釜D中加入的Z最适宜的是 (填编号)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(6)蒸馏塔F中的馏出物T和P分别为 和 ,判断的依据是 。
(7)用该方法合成苯酚和丙酮的优点是 。
Br2和Fe3+ 的水溶液浓度较小时均呈现黄色,二者都具有较强的氧化性。某化学兴趣小组拟通过探究实验来比较二者氧化性的强弱。
实验操作:向足量的硫酸亚铁溶液中加入少量浓溴水,振荡。
实验现象:溶液由浅绿色变为黄色。
(1)提出假设:
甲同学认为氧化性:Br2 >Fe3+ ,则反应的离子方程式为;
乙同学认为氧化性:Fe3+ >Br2 ,则使溶液呈黄色的物质是(填化学式)。
(2)通过进一步实验可以检验甲和乙的结论谁对谁错,下列是设计的一些实验方案和预测:
| 方案 |
实验操作 |
预期现象及结论 |
| 1 |
取少量黄色溶液,加入NaOH溶液 |
若生成红褐色沉淀,则甲正确 |
| 2 |
取少量黄色溶液,加入淀粉KI溶液 |
若溶液变蓝色,则乙正确 |
| 3 |
取少量黄色溶液,加入苯溶液,振荡后静置 |
若上层溶液呈橙红色,则正确 |
①方案1是否合理(填“是”或“否”)。
②方案2中,由于存在反应 (用离子方程式表示),
(用离子方程式表示),
所以预测结论不正确。
③请另外设计一个合理方案,证明已经发生反应。将有关内容填入下表。
| 实验操作 |
预期现象及结论 |
用中和滴定法测定烧碱的纯度,已知烧碱中杂质不与酸反应,试根据要求填空:
(1)配置待测液:称取5.0g烧碱样品,配成250mL待测溶液;
(2)滴定:用0.2000 mol·L-1标准盐酸溶液滴定待测溶液,下面的操作错误的有 。
。
①用标准盐酸溶液润洗酸式滴定管;
②用待测烧碱溶液润洗锥形瓶;
③两个同学合作,一人控制酸式滴定管的活塞,另一人摇动锥形瓶;
④滴定过程中,操作者的眼睛始终注视酸式滴定管液面的变化。
(3)根据下表数据计算:
①待测烧碱溶液的物质的量浓度: (结果保留4位有效数字);
(结果保留4位有效数字);
②烧碱的纯度:。
| 滴定次数 |
待测溶液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读 数(mL) 数(mL) |
||
| 第一次 |
10.00 |
0.50 |
20.45 |
| 第二次 |
10.00 |
4.00 |
24.05 |
17.某同学配置100 ml浓度为1 mol·L-1的Na2CO3溶液,并进行有关实验,请回答下列问题:
(1)需要称量碳酸钠的质量为 ▲g
(2)配置该碳酸钠溶液 时使用的仪器除天平、烧杯、胶头滴管外,还必须用到的玻璃仪器有▲ 、 ▲。
时使用的仪器除天平、烧杯、胶头滴管外,还必须用到的玻璃仪器有▲ 、 ▲。
(3)在操作过程中,该同学转移液体后未经洗涤烧 杯就加水定容至刻度线,则所配置溶液的浓度将
杯就加水定容至刻度线,则所配置溶液的浓度将
▲ (填“偏大”、“偏小”、或“不变”)
(4)在定容这一操作中,应在距刻度线 ▲ 处,改用胶头滴管滴加蒸馏水至容量瓶内液体的▲ 与刻度线保持水平。
孔雀石的主要成 分是CuCO3·Cu(OH)2,还含有少量的SiO2和铁的化合物。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下:
分是CuCO3·Cu(OH)2,还含有少量的SiO2和铁的化合物。实验室以孔雀石为原料制备CuSO4·5H2O的步骤如下: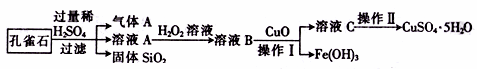
请回答下列问题:
(1)溶液A的金属离子有Cu2+、Fe2+、Fe3+。若要检验溶液A中Fe2+的最适宜选用的试剂为 ____(填代号)。
a.KMnO4 b.铁粉 c.NaCl d.KSCN
(2)向溶液A中加入H2O2的目的是将溶液中的Fe2+氧化为Fe3+,写出该反应的离子方程式:_____________________________________________________;实验室选用H2O2而不用Cl2作氧化剂,除考虑环保因素外,另一原因是_____________________________________。
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发,,过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该 仪器在此操作中的主要作用是。
仪器在此操作中的主要作用是。
(4)将制得的胆矾样品用热重仪进行热重分析,热重仪原理及热重计录如下表:
写出212-248℃温度范围内发生反应的化学方程式:。
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如下图所示的实验装置。请你根据他们的思路,选择下列药品完成实验,填写实验步骤并回答问题。
供选择的药品:铜丝、稀硝酸、烧碱溶液、铁粉、CaCO3颗粒。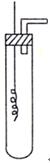
(一)实验步骤:
(1)实验开始时,必须进行的第一步操作是检验装置的;
(2)向试管中加入一定量的固体药品,其目的是;然后向试管中倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞;
(3)反应一段时间后,用蘸有NaOH溶液的棉花团封住导管口;
(4)将铜丝 向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是;
向下移动插入试管液体中,使之与硝酸反应,反应的离子方程式是;
(5)将注射器插入试管口的橡皮塞中,向试管内推入空气,现象是
;
(二)问题探究:分别将等质量的铜片与等体积过量的浓、稀硝酸反应,所得溶液前者
呈绿色、后者呈蓝色,某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确?
(填“正确”或“不正确”),理由是