短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z单质可制成半导体材料,W与X属于同一主族。完成下列有关问题:
(1)元素X的一种核素含10个中子,该核素可表示为________,X的一种氢化物常用来消毒,该氢化物的电子式为________。元素Z在周期表中的位置是________。
(2)元素X和W的简单氢化物中,沸点高的是________(填化学式),理由是________。
(3)请列举两个事实说明元素W的非金属性比Z强: 。
(4)元素X、Y、Z、W形成的二元化合物(指含两种不同元素的化合物)中,化学键的类型相同的一组化合物的化学式是 。
(5)四种元素的原子半径由大到小的顺序是________(填元素符号)。X、Y、W三种元素的原子形成的简单离子中,半径最小的是________(填离子符号)。
元素符号周围不同位置数字的含义 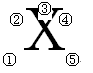
①号位:左下角表示
②号位:左上角表示
③号位:正上方表示
④号位:右上角表示
⑤号位:右下角表示
 的含义
的含义
原子内各种关系
(1)原子序数== =
(2)质量数(A)=+
(3)阳离子:核外电子数= 核电荷数-
(4)阴离子;核外电子数= 核电荷数+
原子是由居于原子中心的和核外构成的。原子核是由带和 构成。
在1911年前后,物理学家卢瑟福把一束变速运动的α粒子(相对原子质量约为4的带2个单位正电荷的质子粒),射向一片极薄的金箔。他惊奇地发现,过去一直认为原子是“实心球”,而由这种“实心球”紧密排列而成的金箔,竟能让大多数α粒子畅通无阻地通过,就像金箔不在那儿似的。但也有极少数的α粒子发生偏转,或被笔直地弹回。根据以上实验现象能得出关于金箔中Au原子结构的一些结论。试写出其中的三点:
(1)______________________________________________________________
(2)______________________________________________________________
(3)______________________________________________________________