300℃时,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:
X(g) +Y(g) 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
| t/min |
2 |
4 |
7 |
9 |
| n(Y)/mol |
0.12 |
0.11 |
0.10 |
0.10 |
回答下列问题:
(1)反应0~2 min Z的平均速率v(Z)=
(2)能判断该反应已经达到平衡状态的是
A.生成X的速率是生成Z的速率的2倍
B.容器内压强保持不变
C.容器内气体的密度保持不变
D.容器内各气体的浓度保持不变
(3)要提高上述反应的转化率,可采取的措施是 (任写一种)。
(4)温度为300℃时,该反应的化学平衡常数K=
(5)若起始时向该容器中充入X、Y、Z各0.20 mol,则反应将向 (填“正”或“逆”)反应方向进行,达平衡时Z的体积分数与上述平衡相比 (填“增大”、“减小”或“不变”)
(15分)铜及其化合物与生产、生活关系密切。
(1)用新制Cu(OH)2与葡萄糖反应制备Cu2O,该反应中葡萄糖是(填“氧化剂”或“还原剂”)
(2)用H2O2稀硫酸共同浸泡废印刷电路板可制备CuSO4若将该反应设计成原电池,
正极的电极反应式为
(3)用NH4NO3氧化海绵铜(含Cu和CuO)生产CuCl的部分流程如下:
①步骤I中,反应温度不宜过高的原因是。
②步骤I中,0.5 mol NH4NO3参加反应有4mol电子转移,铜参与反应的离子方程式为。
③步骤II中,物质X可选用的物质是。(填序号)。
a.Cub.C12c.H2O2d.(NH4)2SO3
④步骤II中物质X需要过量的原因,其一是加快反应速率,其二是_。
⑤步骤II中当NH4 Cl加到一定的量时,生成CuCl 会部分溶解生成CuCl2-在一定温度下建立两个平衡:
Cu Cl(s)  Cu+(a q) + Cl-(a q) Ksp=1.4x10-6
Cu+(a q) + Cl-(a q) Ksp=1.4x10-6
Cu Cl(s) + Cl一(a q) CuCl2(a q) K=0.35
CuCl2(a q) K=0.35
分析[Cu+]、[CuCl2-]和Ksp,K的数学关系,在图中画出「Cu+]、[CuCl2]-的关系曲线(要求至少标出坐标点)
(15分)铝及其化合物用途广泛
(1)铝元素的离子结构示意图为
(2)下列实验能说明Al的金属性(原子失电子能力)小于Na的是(填序号)。
a.分别将Na和Al同时放人冷水中
b.测定等物质的量的Na和A1与酸反应生成H2的体积
c.向Al(OH)3悬浊液中加人足量NaOH溶液
d.用pH计测量NaCl溶液与AlC13溶液的pH
(3)工业上,用冰晶石作助熔剂、石墨作电极电解熔融氧化铝制铝,每生产1吨Al,阳极大约会损失0.6吨的石墨,则石墨被氧化为 (填化学式)。
(4)碳在高温下与Al2O3反应生成Al4C3固体和CO2该反应每转移1 mol电子,吸热a kJ,该反应的热化学方程式为____
(5)室温下,往0.2 mol·L-1 Al2 ( SO4)3溶液中逐滴加人1.0 mol·L-1 NaOH溶液,实验测得溶液pH随NaOH溶液体积变化的曲线如图所示
①a点溶液呈酸性的原因是(用离子方程式表示)_______
②c→d时,A1元素的主要存在形式是(填化学式)
③根据图中数据计算,A1(OH)3的KSP ≈。
利用铜萃取剂M,通过如下反应实现铜离子的富集: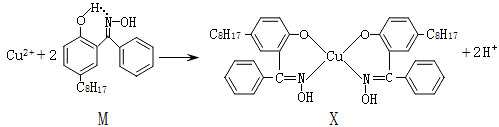
(1)X难溶于水、易溶于有机溶剂,其晶体类型为。
(2)M所含元素的电负性由大到小顺序为,N原子以轨道与O原子形成σ键。
(3)上述反应中断裂和生成的化学键有(填序号)。
a.离子键
b.配位键
c.金属键
d.范德华力
e.共价键
(4)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取。M水溶性小的主要原因是。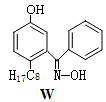
(5)基态Cu2+的外围电子排布式为,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。判断Sc3+、Zn2+的水合离子为无色的依据是。
| 离子 |
Sc3+ |
Ti3+ |
Fe2+ |
Cu2+ |
Zn2+ |
| 颜色 |
无色 |
紫红色 |
浅绿色 |
蓝色 |
无色 |
CuCl是应用广泛的有机合成催化剂,可采取不同方法制取。
方法一铜粉还原CuSO4溶液
已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+ 2Cl- [CuCl3]2-(无色溶液)。
[CuCl3]2-(无色溶液)。
(1)将废铜板浸入热的H2SO4溶液中,并通入空气,可以生成CuSO4。该反应的离子方程式为。
(2)①中,“加热”的目的是,当观察到现象,即表明反应已经完全。
(3)②中,加入大量水的作用是。
(4)潮湿的CuCl在空气中易发生水解和氧化。上述流程中,为防止水解和氧化所添加的试剂或采取的操作是。
方法二铜电极电解饱和食盐水(实验装置如图)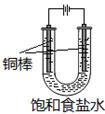
(5)阳极的电极反应式为。
(6)实验开始时,阳极附近没有产生CuOH沉淀的原因是。(已知:Ksp(CuCl)=1.2×10-6,Ksp(CuOH)=1.2×10-14)
I.甲、乙、丙、丁四种物质存在转化关系:
(1)若甲、乙均为空气主要成分,甲所含元素的简单阴离子的结构示意图为。
(2)若乙是生活常见金属单质,丙→丁的离子方程式为。
(3)若丙既能与强酸又能与强碱反应,则丙的化学式为(任写1种)。
II.一定温度下,容积为1 L的密闭容器中投入0.5 mol PCl5(g),存在平衡:PCl5(g) PCl3(g)+ Cl2(g)。反应过程中测得部分数据如下表:
PCl3(g)+ Cl2(g)。反应过程中测得部分数据如下表:
| 时间 |
n(PCl5)/mol |
n(PCl3)/mol |
n(Cl2)/mol |
| 0 |
0.5 |
0 |
0 |
| t1 |
0.45 |
||
| t2 |
0.1 |
||
| t3 |
0.4 |
(4)t1时刻,测得反应吸收的热量为a kJ。PCl3(g)与Cl2(g)反应的热化学反应方程式为。
(5)t2时:v正v逆(填“>”、“<”或“=”)。
(6)相同温度下,改为往容器中投入0.2 mol PCl5(g)、0.2 mol PCl3(g)、0.1 mol Cl2(g),到达平
衡前,PCl5的物质的量将(填“增大”、“减小”、“不变”)。