某课外小组同学设计了如图所示装置(夹持、加热仪器省略)进行系列实验。请根据下列实验回答问题: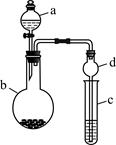
(1)甲同学用此装置验证物质的氧化性:KMnO4>Cl2>Br2,则a中加浓盐酸,b中加KMnO4,c中加_______溶液。将浓盐酸滴入b中后,发生反应的化学方程式是 ;b中反应结束后再向c中加入少量CCl4,振荡静置后观察到c中的现象为________。
(2)乙同学用此装置制少量溴苯,a中盛液溴,b中为铁屑和苯,c中盛水。将液溴滴入b中后,发生反应的化学方程式是:_________, 。向c中滴加AgNO3溶液,可观察到的现象是____________。
(3)丙同学用上述装置制乙酸乙酯,a中加浓硫酸,b中盛装乙醇和乙酸。将浓硫酸滴入b中后用酒精灯对b缓慢加热,b中发生反应的化学方程式是 ;c中应盛装______溶液,其作用是______________________。
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。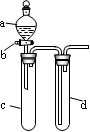
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸,c中反应的化学方程式是_____________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是______。
| 方案 |
反应物 |
| 甲 |
Cu、浓HNO3 |
| 乙 |
Cu、稀HNO3 |
| 丙 |
Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明酸性:HCl>H2CO3>H2SiO3,则分液漏斗a中加入的试剂是___________,c中加入的试剂是_________,d中加入的试剂是_________;实验现象为___________________。
但此实验存在不足之处,改进的措施是___________________________。
使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL)。
Ⅰ.实验步骤:
(1)配制100mL待测白醋溶液。量取10.00mL食用白醋,注入烧杯中用水稀释后转移到___________(填仪器名称)中定容,摇匀即得。
(2)用取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴作指示剂。
(3)读取盛装0.1000 mol/L NaOH 溶液的(填仪器名称)的初始读数。如果液面位置如图所示,则此时的读数为mL。
(4)滴定。当时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
| 滴定次数 实验数据(mL) |
1 |
2 |
3 |
4 |
| V(样品) |
20.00 |
20.00 |
20.00 |
20.00 |
| V(NaOH)(消耗) |
15.95 |
15.00 |
15.05 |
14.95 |
Ⅲ.数据处理与讨论:
(1)经计算,市售白醋总酸量=g/100mL。
(2)在本实验的滴定过程中,下列操作会使实验结果偏大的是(填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
用图示装置制备NO并验证其还原性。
(1)铜与稀硝酸反应的离子方程式是__________。
(2)滴入稀硝酸之前,应该关闭止水夹,点燃红磷并伸入瓶中,塞好胶塞。这样操作的目的是__________。
(3)滴入稀硝酸后,烧杯中的现象是__________。
(4)烧杯中的反应停止后,打开止水夹,通入__________可验证NO的还原性。
探究SO2的性质。甲组同学将SO2分别通入下列3种溶液中。
(1)试管a中观察到的现象是__________。
(2)试管b中观察到紫色褪去,说明SO2具有的性质是__________。
(3)试管c中产生了能溶于稀盐酸的白色沉淀,该白色沉淀是__________。
(4)乙组同学多做了一组实验,他们将SO2通入盛有1.0 mol/L Fe(NO3)3和BaCl2的混合溶液(已知1.0 mol/L Fe(NO3)3溶液中c(H+)=0.1 mol/L)的试管d中,得到了不溶于稀盐酸的白色沉淀。分析产生该白色沉淀的原因:
观点1:SO2与Fe3+反应
观点2:在酸性条件下SO2与 反应
反应
观点3:__________。
欲证明观点2,只需将试管d中Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是__________(填字母)。
a.0.1 mol/L稀硝酸
b.1.5 mol/L Ba(NO3)2和0.1 mol/L HNO3的混合溶液
c.6.0 mol/L NaNO3和0.2 mol/L盐酸等体积混合的溶液
实验室需要65 mL 1.0 mol/L的NaCl溶液用于测定AgNO3溶液的浓度。
(1)用NaCl固体配制NaCl溶液时必须用到的仪器是__________(填序号)。
①天平②烧杯③玻璃棒④酒精灯⑤胶头滴管⑥50 mL容量瓶⑦100 mL容量瓶
(2)需要称取NaCl固体的质量是__________。
(3)量取20 mL AgNO3溶液,当加入25 mL 1.0 mol/L NaCl溶液时恰好完全反应,则c(AgNO3)=____。