甲烷、一氧化碳和氢气、甲醇等既是重要的燃料也是重要的化工原料。
已知:
①2H2(g)+O2(g)===2H2O(l) ΔH1=-571.6 kJ·mol-1
②CH4(g)+ O2(g)===CO(g)+2H2(g) ΔH2=-36 kJ·mol-1
O2(g)===CO(g)+2H2(g) ΔH2=-36 kJ·mol-1
③CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH3=+216 kJ·mol-1
(1)氢气的燃烧热为________,写出甲烷不完全燃烧生成一氧化碳和液态水的热化学方程式: ________________。
(2)现有1 mol由H2O(g)与O2组成的混合气体,且O2的体积分数为x,将此混合气体与足量CH4充分反应。当x=________时,反应②与③放出(或吸收)的总能量为0。若②反应过程中能量转化过程如图所示,下列有关说法中正确的是________。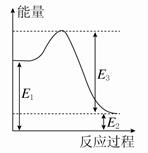
| A.E1=36 kJ | B.E2=36 kJ |
| C.E1-E2=36 kJ | D.E3-E1=36 kJ |
(3)工业上可通过CO和H2化合制得CH3OH:CO(g)+2H2(g)=CH3OH(g) ΔH1(CO结构式为C≡O)。又知某些化学键的键能(断开1 mol化学键时所需要的最低能量)数值如下表:
| 化学键 |
C—C |
C—H |
H—H |
C—O |
C≡O |
H—O |
| 键能 (kJ·mol-1) |
348 |
413 |
436 |
358 |
1072 |
463 |
则ΔH1=_______,在相应的反应条件下,将1 mol CO(g)与足量H2混合充分反应后,放出或吸收的热量 △H1。(用>,<或=填空)
在Cl2、NO、SO2、NO2、NH3五种气体中,与空气相遇能立即变色的是_________;
常用于自来水杀菌、消毒的是________;能用向下排空气法收集的是__________;溶于水后能生成强酸的是_________。
已知在柑橘、柠檬等水果中含有柠檬酸,且已知柠檬酸中只含C、H、O三种元素。 现对该物质进行研究,以测得其结构。
(1)取柠檬酸19.2 g,在氧气中完全燃烧,产生CO2和H2O分别为26.4 g和7.2 g,进行质谱分析,可获得柠檬酸的相对分子质量为192,通过计算,可获得柠檬酸的分子式为____________。
(2)利用__________________分析可知柠檬酸分子中含有—COOH和—OH。
(3)再利用核磁共振氢谱分析发现有4个吸收峰,其峰面积之比为4∶2∶1∶1。综合以上信息,写出柠檬酸的结构简式__________________________________。
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1
则CH4与O2反应生成CO和H2的热化学方程式为_________________;
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。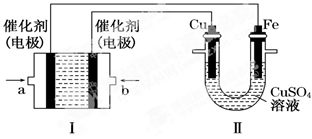
①a处应通入(填“CH4”或“O2”),a处电极上发生的电极反应式是_______________;
②电镀结束后,装置Ⅰ中KOH溶液的浓度(忽略溶液体积的变化)_______(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度________;
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有__________;
④在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8 g,则装置Ⅰ中理论上消耗甲烷________L(标准状况下)。
甲、乙两池电极材料都是铁棒与碳棒,两池中均为饱和NaCl溶液,请回答下列问题: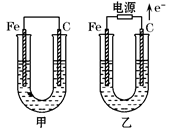
(1)甲池中碳极上电极反应式是________________,甲池铁极上电极反应属于。(填“氧化反应”或“还原反应”)
(2)写出乙池中总反应的离子方程式______________________。
(3)将湿润的淀粉KI试纸放在乙池碳极附近,发现试纸变蓝,待一段时间后又发现蓝色褪去。这是因为过量的Cl2将生成的I2又氧化。若反应的Cl2和I2物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为______________________________。
在2L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ |
600 |
800 |
830 |
1000 |
1200 |
| K |
0.25 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =。
(2)该反应为反应(选填“吸热”、“放热”)。
反应达平衡后,若再通入一定量CO2,则平衡常数K将________,CO2的转化率________。(填“增大”、“减小”或“不变”)
(3)能判断该反应是否达到化学平衡状态的依据是(多选扣分)。
a.容器中压强不变b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O)d.c(CO2)=c(CO)
(4)若 600℃时,向容器中充入1mol CO、1mol H2O,反应达到平衡后,CO的转化率是。