(1)家庭生活中制作食品经常用到碳酸钠(苏打)和碳酸氢钠(小苏打),碳酸氢钠不稳定,在潮湿空气中缓慢分解,受热至65
以上迅速分解,270
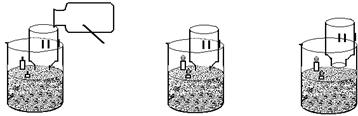
时完全分解为碳酸钠。某同学为探究它们的性质差异,设计了图所示装置并进行实验。请回答:

①加热一段时间后,
两烧杯分别看到的现象是
②碳酸氢钠分解的化学反应方程式:
③该装置设计的优点是
④实验中应注意的问题是
(2)在日常生活和工农业生产中,溶液有着广泛的应用。比如,氨碱工业用到的是饱和食盐水,医疗上使用的则是0.9%的生理盐水。请按要求设计并完成一下实验:
实验用品:氯化钠溶液、氯化钠、硝酸钾、蒸馏水、烧杯、试管、玻璃棒、药匙
探究实验一:澄清透明的氯化钠溶液是否是饱和溶液
| 实验步骤 |
实验现象 |
实验结论 |
| 取一只试管倒入约
氯化钠溶液 ,用药匙加入少量氯化钠固体,振荡,观察现象 |
氯化钠固体溶解 |
探究实验二:将不饱和氯化钠溶液变为饱和溶液并探究饱和氯化钠溶液还能否溶解硝酸钾
| 实验步骤 |
实验现象 |
实验结论 |
|
|
|
不饱和溶液 变为饱和溶液 |
|
|
|
某学生为了证明甲烷中含有碳、氢元素,设计并完成了如下实验方案,请你帮他完成下面的实验报告:
实验目的:证明甲烷中含有碳、氢元素
实验用品:火柴、盛有甲烷的贮气瓶、一个洁净干燥的小烧杯、澄清石灰水
| 实验步骤 |
实验现象 |
结论 |
| ①点燃甲烷 ②将洁净干燥的小烧杯罩在甲烷燃烧的火焰上方 |
证明含有元素 |
|
| ③将蘸有的小烧杯罩在甲烷燃烧的火焰上方 |
证明含有元素 |
请你参与下列探究。
【问题情景】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时,有较多的气泡放出。这一现象激发起同学们的探究欲望,生成的是什么气体呢?
【提出猜想】从物质组成元素的角度分析,放出的气体可能是SO2、O2、H2。
【查阅资料】SO2易溶于水,它能与NaOH溶液反应,生成Na2SO3和H2O。浓硫酸是干燥剂,能吸水。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是。
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量。写出SO2与NaOH反应的化学方程式:。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。
如果放出的是O2和H2的混合物,你认为方案中的安全隐患是。
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指,若不发出 ,方可采用上面的装置进行实验。
【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量不变。
结论:(4)铁粉与硫酸铜溶液反应时,产生的气体是 。
(5)写出H2还原CuO的化学方程式:。
【思维拓展】
(6)不通过称量,如何判断SO2与NaOH溶液发生了反应呢?有一同学设计了下图所示的装置进行实验,
发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论。其他同学认为这一方案不严谨,理由是 。
如下图A所示,取一个大烧杯,在里面装入约1/2的细沙;烧杯一边的细沙中,插入高低不同的两支蜡烛;将截取瓶底的大口饮料瓶做成简易漏斗,取三张用石蕊溶液染成紫色的干燥小纸条,将一张干燥的和一张润湿后的纸条(润湿后仍为紫色)粘在简易漏斗的内壁,将另一张纸条润湿后,粘在简易漏斗的外壁,将漏斗插入细沙的另一边。按下列各步骤继续实验,并回答有关问题。
|
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究,请填写以下探究过程中的空格:(提示:稀盐酸与石灰石反应生成二氧化碳和水、氯化钙;与氢氧化钠反应生成水和氯化钠)
(1)提出假设:化学反应中,反应物的总质量与生成物的总质量 。
(2)确定研究方法:分析推理,查阅资料,实验探究。
(3)设计并进行实验:小刚设计的实验装置和选用药品如图A所示,小洁的如图B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。
(4)实验结论:通过实验,小刚认为:在化学反应中,生成物的总质量与反应物的总质量不相等,小洁认为:在化学反应中,生成物的总质量与反应物的总质量相等,你认为结论正确的是① ,请你谈谈导致另一种结论错误的原因:② 。
(5)结论分析:请从原子的角度,简要分析你认为正确结论的依据:
在化学反应前后原子的①、②、
③不变。
(6)查阅资料:小刚和小洁通过查阅资料了解到:法国伟大的科学家拉瓦锡,早在18世纪就围绕这个问题,进行了准确,缜密的研究,并做出了科学结论。
为了让学生完成“证明分子间有空隙”的家庭实验,老师已给每位同学准备了一只有刻度的小烧杯,则同学们回家后还需要准备 、 、 。
实验步骤是:
⑴
⑵
实验现象是
得出的结论是