①~⑩十种元素,在元素周期表中的位置如图所示。回答下列问题:
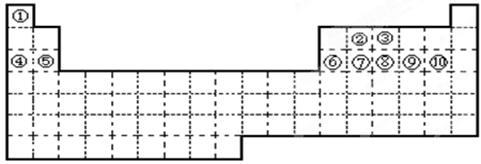
(1)在上述十种元素中,置换酸中氢的能力最强的元素为 (填化学符号,下同);最高价氧化物的水化物的酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是 ,显两性的氢氧化物的化学式是 ;原子半径最大的元素是 ,半径最小的离子是 。
(2)上述十种元素中,金属性最强的元素在周期表中的位置是第 周期 族,该元素的单质在空气中燃烧的化学方程式为 。
(3)试用电子式表示元素①和③形成分子的过程 。
(16分)尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
⑴工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为。
⑵当氨碳比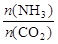 =4时,CO2的转化率随时间的变化关系如右图所示。
=4时,CO2的转化率随时间的变化关系如右图所示。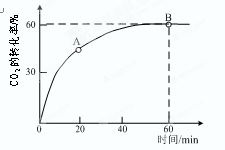
①A点的逆反应速率v逆(CO2)B点的正反应速率v正(CO2)(填 “大于”、“小于”或“等于”)
②NH3的平衡转化率为。
⑶人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如右图。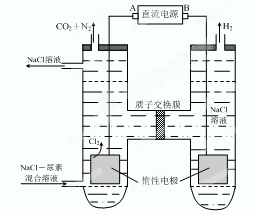
①电源的负极为(填“A”或“B”)。
②阳极室中发生的反应依次为、。
③电解结束后,阴极室溶液的pH与电解前相比将;若两极共收集到气体13.44 L(标准状况),则除去的尿素为g(忽略气体的溶解)。
已知:N2O4(g) 2NO2(g)ΔH=+52.70 kJ·mol—1。
2NO2(g)ΔH=+52.70 kJ·mol—1。
(1)在恒温、恒容的密闭容器中进行上述反应时,下列描述中能说明该反应已达平衡的是。
a.v(N2O4)正=2 v(NO2)逆
b.容器中气体的平均相对分子质量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(2)t℃恒温下,在固定容积为2L的密闭容器中充入0.054 mol N2O4,半分钟后达到平衡,测得容器中含n(NO2)=0.06 mol,则v(NO2) =,t℃时反应N2O4(g) 2NO2(g)的平衡常数K=。若向容器内继续通入少量N2O4,则平衡移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后NO2的体积分数原平衡时NO2的体积分数(填“大于”、“小于”或“等于”)。
2NO2(g)的平衡常数K=。若向容器内继续通入少量N2O4,则平衡移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后NO2的体积分数原平衡时NO2的体积分数(填“大于”、“小于”或“等于”)。
(3)取五等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g) N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是。
N2O4(g)。反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是。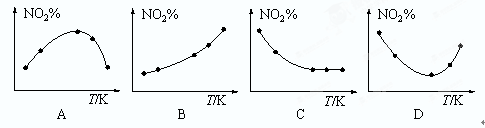
由方铅矿(PbS)制备Pb和PbO2的方法如下: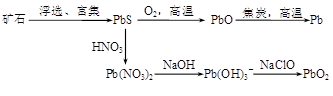
PbO与焦炭煅烧时可能会发生如下反应:
PbO(s)+C(s)=Pb(s)+CO(g) ΔH=+108.5 kJ·mol—1 ①
PbO(s)+CO(g)=Pb(s)+CO2(g) ΔH=-64 kJ·mol—1 ②
(1)已知Pb与O2反应的热化学方程式为:2Pb(s)+O2(g)=2PbO(s) ΔH=-438 kJ·mol—1
则C完全燃烧的热化学方程式为。
(2)能提高反应②中PbO转化率的措施有(填字母)。
a.升高温度 b.增大压强 c.加入焦炭 d.加入催化剂
(3)制备过程中会产生SO2、NO、CO等有毒气体,可将它们按一定比例混合在一定条件下反应得到S、N2和CO2。若SO2与NO的体积比为1∶2,该反应的化学方程式为。
(4)水溶液中铅的存在形态有多种,各形态的浓度分数α随溶液pH变化的关系如下图所示: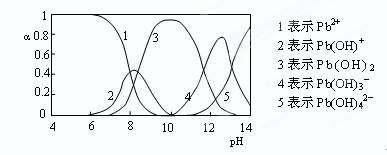
pH=6.5时,Pb2+水解的离子方程式为;加入NaClO制备PbO2之前需先用NaOH调节溶液pH至12.5,理由是。
下列框图涉及到的物质所含元素中,除一种元素外,其余均为1~18号元素。已知:A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列全)。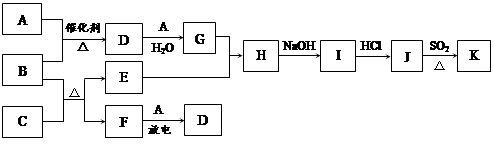
请回答下列问题:
(1)B的电子式为。
(2)J、K是同种金属的氯化物,且K为白色沉淀。写出SO2还原J生成K的离子方程式。
(3)汽车尾气中常含有D。B与D在加热和催化剂存在的条件下,发生反应生成两种对空气无污染的物质。请写出该反应的化学方程式。
(4)有人认为:“表面化学”研究成果能使B和D的反应在催化剂表面进行时的效率大大提高,从而使污染物D的转化率大大提高。请你应用化学基本理论对此观点进行评价:。
活性ZnO在橡胶、塑料、涂料工业中有重要应用,一种由粗ZnO(含FeO、CuO)制备活性ZnO的流程如下(已知:碱式碳酸锌经焙烧可制得活性ZnO):
已知:几种离子生成氢氧化物沉淀时的pH如下表:
| 待沉淀离子 |
Fe2+ |
Fe3+ |
Zn2+ |
Cu2+ |
| 开始沉淀时pH |
6.34 |
1.48 |
6.2 |
5.2 |
| 完全沉淀时pH |
9.7 |
3.2 |
8.0 |
6.4 |
请问答下列问题:
⑴步骤A加H2O2发生反应的离子方程式是,该步骤需控制溶液pH的范围是。
⑵ A溶液中主要含有的溶质是。
⑶碱式碳酸锌经焙烧制得活性ZnO的反应△H>0,该反应能自发进行的原因是。
⑷若经处理后的废水pH=8,此时Zn2+的浓度为mg/L(常温下,Ksp[Zn(OH)2]=1.2×10-17)。