某合金与铁的物理性质的比较如下表所示:
| |
熔点/℃ |
密度/ g·cm-3 |
硬度(金刚石为10) |
导电性(银为100) |
| 某合金 |
2 500 |
3.00 |
7.4 |
2.3 |
| 铁 |
1 535 |
7.86 |
4.5 |
17 |
还知该合金耐腐蚀,强度大,从以上性能看,该合金不适合作
A.导线 B.门窗框 C.炉具 D.飞机外壳
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=﹣49.0kJ·mol﹣1.一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是
CH3OH(g)+H2O(g)△H=﹣49.0kJ·mol﹣1.一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是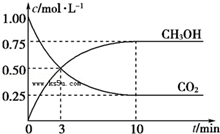
| A.欲增大平衡状态时c(CH3OH)/c(CO2)的比值, 可采用 升高温度的方法 |
| B.3 min时,CO2的消耗速率等于CH3OH的生成速率,且二者浓度相同 |
| C.欲提高H2的平衡转化率只能减小反应容器的体积 |
| D.从反应开始到平衡,CO2的平均反应速率v(CO2)="0.025" mol·L﹣1·min﹣1 |
已知:NO2(g)+SO2(g) SO3(g)+NO(g),现将体积之比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
SO3(g)+NO(g),现将体积之比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
| A.体系压强保持不变 |
| B.混合气体颜色保持不变 |
| C.SO3与NO的体积比保持不变 |
| D.每消耗1molSO2,同时生成1molNO |
根据反应:S2O32﹣+2H+═SO2+S↓+H2O,下表各组实验最快出现浑浊的是
| Na2S2O3溶液 |
稀H2SO4 |
H2O |
温度/℃ |
|||
| c(mol·L﹣1) |
V(mL) |
c(mol·L﹣1) |
V(mL) |
V(mL) |
||
| A |
0.1 |
5 |
0.1 |
5 |
5 |
10 |
| B |
0.2 |
5 |
0.1 |
5 |
10 |
10 |
| C |
0.1 |
5 |
0.1 |
5 |
10 |
30 |
| D |
0.2 |
5 |
0.1 |
5 |
10 |
30 |
对已达化学平衡的反应:2X(g)+Y(g) 2Z(g),减小压强后,对反应产生的影响是
2Z(g),减小压强后,对反应产生的影响是
| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正反应速率先减小后增大,逆反应速率减小,平衡向逆反应方向移动 |
| D.逆反应速率先减小后增大,正反应速率减小,平衡向逆反应方向移动 |
CO(g)+NO2(g) CO2(g)+NO(g)△H<0,若其他条件不变,只改变下列条件,能使混合气体颜色变深的是
CO2(g)+NO(g)△H<0,若其他条件不变,只改变下列条件,能使混合气体颜色变深的是
| A.降低温度 | B.使用催化剂 |
| C.增大CO的浓度 | D.增大压强 |