N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 。
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g) 4NO2(g)+O2(g);ΔH>0
4NO2(g)+O2(g);ΔH>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将 (填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s |
0 |
500 |
1000 |
| c(N2O5)/mol·L-1 |
5.00 |
3.52 |
2.48 |
则500 s内N2O5的分解速率为 。
③在T2温度下,反应1000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1(填>、<或=)。
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2。
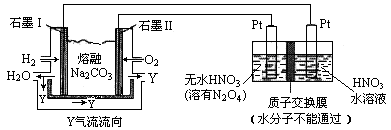
写出石墨Ⅰ电极上发生反应的电极反应式 ,N2O5在电解池的 区生成(填“阳极”或“阴极”)。
2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是。
(2)在由水电离产生的c(H+)=1×10-14 mol·L-1的溶液中,①NH4+、Al3+、Br-、SO42-② Na+、Mg2+、Cl-、NO3-③K+、Ba2+、Cl-、NO3-④K+、Na+、HCO3-、SO42-四组离子中,一定可以大量共存的是(填序号,下同),可能大量共存的是。
(3)在下列反应中,水仅做氧化剂的是(填字母,下同),水既不做氧化剂又不做还原剂的是。
| A.Cl2+H2O=HCl+HClO |
| B.2Na2O2+2H2O=4NaOH+O2↑ |
| C.CaH2+2H2O=Ca(OH)2+2H2↑ |
D.3Fe+4H2O Fe3O4+4H2 Fe3O4+4H2 |
(4)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为。
(5)右图是某品牌饮用矿泉水标签的部分内容。请认真阅读标签内容后计算。
①该矿泉水中镁离子的物质的量浓度的最大值是;
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过mol。
如图,E为沾有Na2SO4溶液的滤纸,并加入几滴酚酞。A,B分别为Pt片,压在滤纸两端,R、S为电池的电极。M、N是用多微孔的Ni的电极材料,它在碱溶液中可以视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央点上一滴紫色的KMnO4溶液,K打开,接通电源一段时间后,C、D中有气体产生。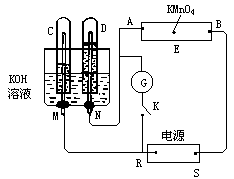
(1)外电源的正、负极分别是R为____,S为_____。
(2)A附近溶液的现象是_______,B附近发生的电极反应式为
(3)滤纸上的紫色点向哪方移动____。
(4)当C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,主要因为____,有关的反应式为_____。
工业上主要采用电解饱和食盐水的方法来制取Cl2、H2、NaOH。请回答下列问题:
(1)在电解过程中,所发生反应的离子反应方程式为:;
(2)电解之前食盐水需要精制,目的是除去粗盐的中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:a、Na2CO3溶液 b、Ba(OH)2溶液 c、稀盐酸。其中合理的加入顺序为(填写序号) ;
(3)如果在容积为10L的电解池内,一段时间后共收集到11.2L(标准状况)气体。这时溶液中NaOH的物质的量浓度为(设电解时溶液的体积不变)。
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。请回答下列问题: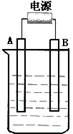
(1)A接的是电源的极,B是该装置。
(2)写出电解时反应的总离子方程式。
(3)电解后溶液的pH为;要使电解后溶液恢复到电解前的状态,则需加入,其质量为。(假设电解前后溶液的体积不变)
已知在298K时下列反应的反应热为:
(1)CH3COOH(l) + 2O2(g)=2CO2(g)+2H2O (l) △H1=-870.3KJ/mol
(2)C(s)+O2(g)=CO2(g) △H2=-393.5KJ/mol
(3)H2(g)+1/2O2(g)=H2O (l)△H3=-285.8KJ/mol
试计算下述反应的反应热:
2C(s) +2H2(g) +O2(g) =CH3COOH(l)