硫酸铜在生产、生活中应用广泛。某化工厂用含少量铁的废铜渣为原料生产胆矾的流程如下:
(1)写出浸出时铜与稀硫酸、稀硝酸反应生成硫酸铜的化学方程式:______________。
(2)取样检验是为了确认Fe3+是否除净,你的检验方法是__________。
(3)滤渣c是_________。
(4)气体a可以被循环利用,用化学方程式表示气体a被循环利用的原理为2NO+O2===2NO2、_________。
(5)一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,且n(SO3)∶n(SO2)=1∶2,写出硫酸铜受热分解的化学方程式:______________。
某同学设计了如下图所示的实验装置分别测定生成的SO2、SO3气体的质量和O2气体的体积。此设计有不合理之处,请说明理由:______________。
二氧化铈CeO2是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下: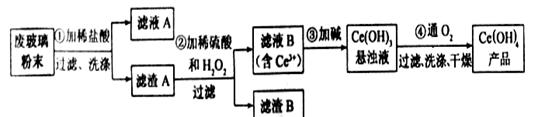
(1)洗涤滤渣A的目的是为了去除(填离子符号),检验滤渣A是否洗涤干净的方法是。
(2)第②步反应的离子方程式是,滤渣B的主要成分是。
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP(填“能”或“不能”)与水互溶。实验室进行萃取操作是用到的主要玻璃仪器有、烧杯、量筒等。
(4)取上述流程中得到的Ce(OH)4[M=208g/mol]产品0.500g,加硫酸溶解后,用0.1000mol•L-1FeSO4标准溶液滴定(铈被还原为Ce3+),消耗20.00mL标准溶液,该产品中Ce(OH)4的质量分数为。(保留两位小数)
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示: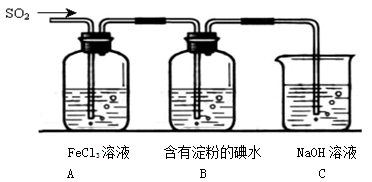
(1)装置C的作用是
(2) 若要从FeSO4溶液获得FeSO4•7H2O晶体,必须进行的实验操作步骤:、、过滤、洗涤、自然干燥。
(3)根据以上现象,该小组同学认为SO2与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式;
②请写出检验A烧杯中有Fe2+生成的操作方法;
③该小组同学向C烧杯反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法(填“合理”或“不合理”),理由是。
(4)能表明I-的还原性弱于SO2的现象是。
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下: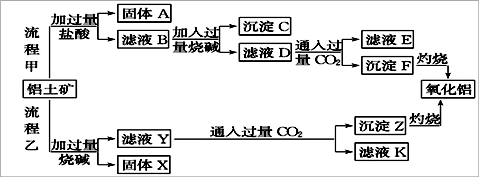
请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为:;
(2)流程乙加入烧碱后生成SiO32-的离子方程式为______。
(3)验证滤液B含Fe3+,可取少量滤液并加入______(填试剂名称)。
(4)滤液E中溶质的主要成分是____(填化学式),写出该溶液的一种用途。
化学兴趣小组的同学设计实验探究浓硫酸与木炭反应后产生气体的成分。
(1)写出浓硫酸与木炭反应方程式,并标明电子转移的方向和数目:____________________。
【装置设计】组装如下的实验装置,然后进行实验探究。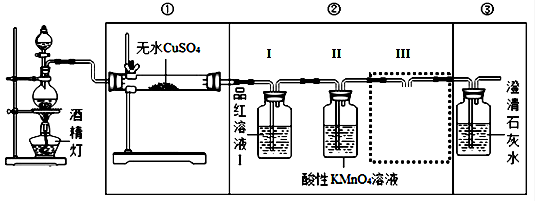
(2)装入反应物之前,必须先。
(3)要验证产生的气体中含有CO2,请在答题卡中完成图中虚线框内的装置简图,并标明试剂。
【实验探究】
(4)观察实验,完成实验现象的部分记录:
| 实验装置 |
① |
② |
③ |
| 实验现象 |
…… |
(5)实验装置②中品红溶液Ⅰ的作用,III的作用。
净水剂液体聚合硫酸铝铁兼具铁盐和铝盐的双重絮凝特性,一般是以铁盐为主,铝盐为辅。现用的铝土矿(其主要成分是Al2O3,含有少量杂质Fe2O3和SiO2,其他杂质忽略不计)来制备该净水剂,其工艺流程如下: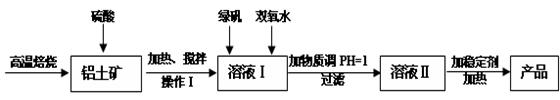
(1)H2SO4浓度的适宜范围是45%~50%,反应的适宜温度是100℃,其目的是:;Al2O3与H2SO4反应的化学反应方程式是__________。
(2)操作I为:冷却静置、、洗涤,所得到的溶液I中的金属阳离子有_______(填化学式)。
(3)溶液I中加入绿矾(FeSO4·7H2O)和双氧水的目的是:,涉及的反应离子方程式为__。
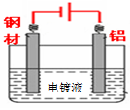
(4)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,请在答题卡中完成钢材镀铝的装置示意图,并作相应标注。