分类方法在化学学科的发展中起到了非常重要的作用。下列分类标准合理的是
①根据碳酸钠溶于水呈碱性,碳酸钠既属于盐,又属于碱
②根据反应中是否有电子的转移,将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和悬浊液
④根据反应中是否有离子反应参与,将反应分为离子反应和非离子反应
| A.①③ | B.②④ | C.①④ | D.③④ |
下列表示对应化学反应的离子方程式正确的是( )
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3—+3H2O=3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-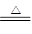 NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中:SO2+NH3·H2O=HSO3—+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3—=Ag++NO↑+H2O |
下列离子方程式正确的是( )
| A.利用醋酸溶解含碳酸钙的水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
B.用铜为电极电解饱和食盐水:2Cl-+2H2O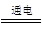 Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.在明矾溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2—+4NH4++2H2O |
| D.在小苏打溶液中加少量Ba(OH)2溶液:2HCO3—+Ba2++2OH-=BaCO3↓+2H2O+CO32— |
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3—、N2、Cl-六种物质。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是( )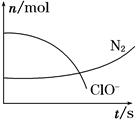
| A.还原剂是含CN-的物质,氧化产物只有N2 |
| B.氧化剂是ClO- , 还原产物是HCO3— |
| C.配平后氧化剂与还原剂的化学计量数之比为5∶2 |
| D.若生成2.24 L N2(标准状况),则转移电子0.5 mol |
做好环境消毒工作是预防“禽流感”的重要措施,常用的一种消毒剂是ClO2,实验室可通过以下反应制得ClO2(未配平):KClO3+H2C2O4+H2SO4―→ClO2↑+K2SO4+CO2↑+H2O。下列说法正确的是( )
| A.H2SO4在反应中作氧化剂 |
| B.ClO2是氧化产物 |
| C.H2C2O4在反应中被氧化 |
| D.1 mol KClO3参加反应时有2 mol电子转移 |
乙醇与重铬酸根离子在酸性溶液中能发生如下反应:C2H5OH+Cr2O72—+H+―→CO2↑+Cr3++H2O,当这个方程式配平后,H+的化学计量数为( )
| A.10 | B.12 | C.14 | D.16 |