某强酸性溶液X含有Ba 2+ 、Al 3+ 、NH4+、Fe 2+ 、Fe 3+ 、CO32-、SO32-、SO42-、Cl-、
NO3-中的一种或几种,取该溶液进行实验,实验内容如下:

根据以上信息,回答下列问题:
(1)溶液X中除H + 外还肯定含有的离子是 ;不能确定是否含有的离子是 ,若要确定其中阳离子的存在,最可靠的化学方法是 。
(2)沉淀G的化学式为 。
(3)写出有关离子方程式:
步骤①中生成A 。
步骤②生成沉淀I 。
(4)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H + )="0.04" mol,而沉淀C物质的量0.07 mol,能说明(1)中不能确定的阴离子存在的理由是 。
某化学反应的反应物和产物如下:
KMnO4+ KI+ H2SO4→ MnSO4 + I2 + KIO3+ K2SO4 + H2O
(1)该反应的氧化剂是。
(2)如果该反应方程式中I2和KIO3的化学计量数都是5
①KMnO4的化学计量数是。
②在下面的化学式上标出电子转移的方向和数目
KMnO4+ KI + H2SO4 →
(3)如果没有对该方程式中的某些化学计量数作限定,可能的配平化学计量数有许多组。原因是。
(10分) 容积固定的密闭容器中,发生可逆反应:M(g)+N(g)  2P(g)+Q(g) ΔH>0,
2P(g)+Q(g) ΔH>0,
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1 mol·L-1,c(N)=2.4 mol·L-1,达到平衡后,M的转化率为60%,此时N 的浓度是,P 的体积分数为_________。
(2)若反应温度升高,M的转化率____________ (填“增大”“减小”或“不变”,下同),平均相对分子质量____________,混合气体密度____________。
(12分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)  CH3OH(g),不同温度时甲醇的物质的量随时间变化曲线如下图所示。根据题意完成下列各题:
CH3OH(g),不同温度时甲醇的物质的量随时间变化曲线如下图所示。根据题意完成下列各题: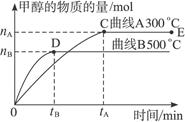
(1)反应达到平衡时,升高温度,v正_____________ (填“增大”“减小”或“不变”)。化学平衡向移动
(2)500 ℃,从反应开始到平衡,H2的反应速率v(H2)=________________________。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是_____________。
| A.氢气的浓度减小 | B.正反应速率加快,逆反应速率也加快 |
| C.甲醇的物质的量增加 | D.重新平衡时n(H2)/n(CH3OH)增大 |
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是__________________________(用化学方程式表示)。
反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
(1)该反应是_____________(填“吸热”“放热”)反应。
(2)当反应达到平衡时,升高温度,A的转化率_____________ (填“增大”“减小”或“不变”),
原因是_________________________________________________________________。
(3)反应体系中加入催化剂对反应热是否有影响并说明原因_________________________
___________________________________________。
(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_____________,E2_____________ (填“增大”“减小”或“不变”)。
由金红石(TiO2)制取单质Ti,涉及的步骤为: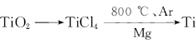
已知:①C(s)+O2(g)====CO2(g) ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g) ====2CO2(g) ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g) ====TiCl4(s)+O2(g) ΔH="+141" kJ·mol-1
则(1)TiO2(s)+2Cl2(g)+2C(s) ====TiCl4(s)+2CO(g)的ΔH=____________________。
(2)碳在氧气中不完全燃烧生成CO的热化学方程式为_______________________________。