已知反应:mX(g)+nY(g)  qZ(g) ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法中正确的是
qZ(g) ΔH<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法中正确的是
| A.通入稀有气体使压强增大,平衡将向正反应方向移动 |
| B.X的正反应速率是Y的逆反应速率的m/n倍 |
| C.降低温度,混合气体的平均相对分子质量变小 |
| D.增加X的物质的量,Y的转化率降低 |
右图是关于反应A2(g)+3B2(g)===2C(g)△H<0的平衡移动图形,影响平衡移动的原因是()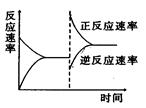
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时使用催化剂; |
| D.增大反应物浓度,同时减小生成物浓度 |
对于3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
已知(l)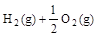 =H2O(g)△H1=a kJ·
=H2O(g)△H1=a kJ·
(2)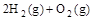 =2H2O(g)△H2=b kJ·
=2H2O(g)△H2=b kJ·
(3)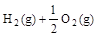 =H2O(l)△H3=c kJ·
=H2O(l)△H3=c kJ·
(4) =2H2O(l)△H4=d kJ·
=2H2O(l)△H4=d kJ·
下列关系式中正确的是()
| A.a<c<0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
实验室进行中和热测定的实验时除需要大烧杯(500 mL)、小烧杯(100 mL)外,所用的其他仪器和试剂均正确的一组是( )
| A.0.50 mol·L-1盐酸,0.50 mol·L-1NaOH溶液,100 mL量筒1个 |
| B.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,100 mL量筒2个 |
| C.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒1个 |
| D.0.50 mol·L-1盐酸,0.55 mol·L-1NaOH溶液,50 mL量筒2个 |
下列与化学反应能量变化相关的叙述正确的是( )
| A.生成物总能量一定低于反应物总能量 |
| B.等量H2在O2中完全燃烧,生成H2O(g)与生成H2O(l)放出的能量相同 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同 |