(共10分)如图表示反应N2(g)+3H2(g)  2NH3(g); △H<0 在某一时间段反应速率与反应过程的曲线关系图,
2NH3(g); △H<0 在某一时间段反应速率与反应过程的曲线关系图,
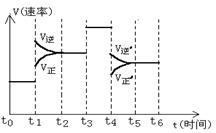
①达到平衡后,若只改变一个条件,则t1条件为 ;t3条件为 ;t4条件为 ;
②则图中氨的百分含量最低的时间段是:( )
| A.t0-t1 | B.t2-t3 | C.t3-t4 | D.t5-t6 |
③请在右图中画出t6时刻既增加氢气浓度同时又减小氨气浓度的速率随时间的变化图。
由黄铜矿(主要成分是
)炼制精铜的工艺流程示意图如下:
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000℃左右,黄铜矿与空气反应生成
和
的低价硫化物,且部分
的硫化物转变为低价氧化物。该过程中两个主要反应的化学方程式分别是、,反射炉内生成炉渣的主要成分是;
(2)冰铜(
和
互相熔合而成)含
量为20%--50%。转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的
被氧化为
,生成
与
反应,生成含
量约为98.5%的粗铜,该过程发生反应的化学方程式分别是、;
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极(填图中的字母);在电极
上发生的电极反应式为;若粗铜中还含有
,它们在电解槽中的存在形式和位置为。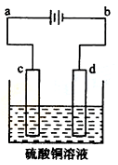
光气(
)在塑料、制革、制药等工业中有许多用途,工业上采用高温下
与
在活性炭催化下合成。
(1)实验室常用来制备氯气的化学方程式为
(2)工业上利用天然气(主要成分为 )与 进行高温重整制备 ,已知 、 、和 的燃烧热( )分别为-890.3 、-285.8 和-283.0 ,则生成1 (标准状况) 所需热量为
(3)实验室中可用氯仿(
)与双氧水直接反应制备光气,其反应的化学方程式为
(4)
的分解反应为
。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10
到14
的
浓度变化曲线未示出):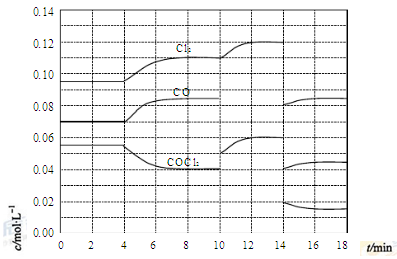
①计算反应在第8
时的平衡常数
=
②比较第2
反应温度
(2)与第8
反应温度
(8)的高低:
(2)
(8)
(填"<"、">"或"="),
③若12
时反应于温度
(8)下重新达到平衡,则此时
=
;
④比较产物
在2-3
、5-6
和12-13
时平均反应速率(平均反应速率分别以v(2-3)、v(5-6)、v(12-13))的大小
⑤比较反应物 在5-6 和15-16 时平均反应速率的大小:v(5-6)v(15-16)(填"<"、">"或"="),原因是
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物
的化学式,可用离子交换和滴定的方法。实验中称取0.54
的
样品,溶解后先进行阳离子交换预处理,再通过含有饱和
的阴离子交换柱,使
和
发生交换。交换完成后,流出溶液的
用0.40
的盐酸滴定,滴至终点时消耗盐酸25.0
。计算该样品中氯的物质的量,并求出
中
值:(列出计算过程);
(2)现有一含有
和
的混合物样品,采用上述方法测得
=1:2.1,则该样品中
的物质的量分数为。在实验室中,
可用铁粉和盐酸反应制备,
可用铁粉和反应制备;
(3)
与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(4)高铁酸钾( )是一种强氧化剂,可作为水处理剂和高容量电池材料。 与 在强碱性条件下反应可制取 ,其反应的离子方程式为与 电池类似, - 也可以组成碱性电池, 在电池中作为正极材料,其电极反应式为,该电池总反应的离子方程式为。
揖选做题铱本题包括
、
两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按
小题评分。
A.一项科学研究成果表明,铜锰氧化物(
)能在常温下催化氧化空气中的一氧化碳和甲醛(
)。
(1)向一定物质的量浓度的
和
溶液中加入
溶液,所得沉淀经高温灼烧,可制得
。
①
基态的电子排布式可表示为。
②
的空间构型是(用文字描述)。
(2)在铜锰氧化物的催化下,
被氧化为
,
被氧化为
和
。
①根据等电子体原理,
分子的结构式为。
②
分子中O 原子轨道的杂化类型为。
③1
中含有的σ键数目为。
(3) 向
溶液中加入过量
溶液可生成
。不考虑空间构型,
的结构可用示意图表示为。
铝是地壳中含量最高的金属元素,其单质及合金在生产生活中的应用日趋广泛。
(1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,其相关反应的热化学方程式如下:
①反应
的
=kJ·mol-1(用含
、
的代数式表示)。
②
是反应过程中的中间产物。
与盐酸反应(产物之一是含氢量最高的烃) 的化学方程式为。
(2)镁铝合金(
)是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的
、
单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
。得到的混合物
(
)在一定条件下可释放出氢气。
①熔炼制备镁铝合金(
)时通入氩气的目的是。
②在
溶液中,混合物
能完全释放出
。1 mol
完全吸氢后得到的混合物
与上述盐酸完全反应,释放出
的物质的量为。
③在
和
溶液中,如图混合物
均只能部分放出氢气,反应后残留固体物质的
射线衍射谱图如图所示(
射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。在上述
溶液中,混合物
中产生氢气的主要物质是(填化学式)。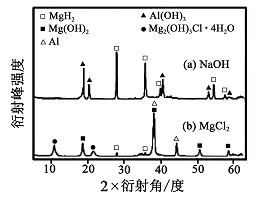
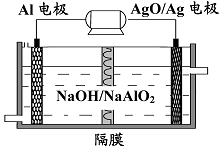
(3)铝电池性能优越,
电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为。