已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH CH3COO‾+H+ ΔH>0。
CH3COO‾+H+ ΔH>0。
(1)常温常压下,在 pH =5的稀醋酸溶液中,c(CH3COO‾)=_________;下列方法中,可以使0.10 mol·L‾1CH3COOH的电离程度增大的是___________。
a.加入少量0.10 mol·L‾1的稀盐酸
b.加热CH3COOH溶液
c.加入少量冰醋酸
d.加水稀释至0.010 mol·L‾1
e.加入少量氯化钠固体
f.加入少量0.10 mol·L‾1的NaOH溶液
(2)将等质量的锌投入等体积且pH均等于3的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_________V(醋酸),反应的最初速率为:υ(盐酸)_________υ(醋酸)。
(3)常温下,向体积为Va mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液Vb mL至溶液恰好呈中性,则Va与Vb的关系是:Va____Vb。
(4)已知:90℃时,水的离子积常数为Kw = 38×10‾14,在此温度下,将pH=3的盐酸和pH = 11的氢氧化钠溶液等体积混合,则混合溶液中的c(H+)=__________(保留三位有效数字)。
A、B、C、D四种短周期元素,A、B同主族,C、D同周期。气体A2与气体C2按体积比2:1混和后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B的阳离子与C的阴离子的核外电子排布相同。D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
(1)写出A、B、C三种元素的名称:A;B ;C;D在周期表中的位置是。
(2)写出化合物B2C2的电子式。
(3)写出B2C2和A2C反应的离子方程式:。
(4)用电子式表示A2C形成的过程:。
(1)如右图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_______________。
(2)乙烷中含有乙烯除杂试剂为;
反应的化学方程式为。
(3)在10L密闭容器中充入2molA和1molB,发生的化学反应:3A(g)+B(g)  C(g)
C(g)
+2D(g),2min后反应达到平衡,在相同温度下,测得平衡时容器内气体的压强是反应前的5/6,试填写下列空白:
①用气体B表示的2min内的平均反应速率为。
②平衡时,A的浓度为mol/L。
(4)我国拥有完全自主产权的氢氧燃料电池车在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。电池负极反应为,
正极反应。
将下列物质进行分类:①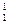 H与
H与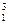 H②O2与O3③
H②O2与O3③ 乙醇与甲醚(CH3—O—CH3)④H2O与D2O⑤CH3CH2CH2CH2
乙醇与甲醚(CH3—O—CH3)④H2O与D2O⑤CH3CH2CH2CH2 CH3与CH3-CH(CH3)-CH3⑥C60与C70
CH3与CH3-CH(CH3)-CH3⑥C60与C70
(1)互为同位素的是(填编号、下同);
(2)互为同素异形体的是;
(3)互为同分异构体的是;
(4)互为同系物的是。
A、B、C、D、E、F六种物质在一定条件下有如下图所示的相互转化关系,所有反应物和生成物均已给出。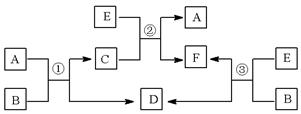
(1)若反应①、②、③均为溶液中的置换反应,A、D、E为第ⅦA族元素单质。则A、D、E的氧化性由强到弱的顺序为(用化学式表示)________________________。
(2)若B是某元素R的氢化物,B的沸点大于与其同主族的其他元素氢化物的沸点,且B在常温下为液态;C是一种有磁性的化合物;E是一种无色、无味的有毒气体。则反应①的化学方程式___________________,③的化学方程式______________。
(3)若B由短周期元素X、Y组成,且X、Y原子个数比为1∶1,B晶体中既含离子键,又含非极性共价键;绿色植物的光合作用和呼吸作用可实现自然界中 D、E的循环。则B的电子式为_________________,反应①的离子方程式_____________________________。
D、E的循环。则B的电子式为_________________,反应①的离子方程式_____________________________。
甲、乙、丙为常见单质,乙、丙两元素在周期表中位于 同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答:
同一主族。X、A、B、C、D、E、F、G均为常见的化合物,其中A和X的摩尔质量相同,A、G的焰色反应为黄色。在一定条件下,各物质相互转化关系如右图。请回答: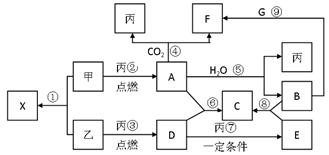
(1)写化学式:丙_____E________
(2)X的电子式为_____________。
(3)写出反应⑥的化学反应方程式:。
(4)写出B与G溶液反应生成F的离子方程式:。
(5)在上图的反 应中,不属于氧化还原反应的是(填序号)____________________。
应中,不属于氧化还原反应的是(填序号)____________________。
(6)将8 g乙在足量丙中燃烧,所得气体D通入100mL 3.5mol·L-1的B溶液中,完全吸收 后,溶液中的溶质及其物质的量分别为;若同体积的气体D通入100mL 2.5mo
后,溶液中的溶质及其物质的量分别为;若同体积的气体D通入100mL 2.5mo l·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为。
l·L-1的B溶液中,完全吸收后,溶液中所含离子的物质的量浓度由大到小的顺序为。