近年来高铁酸钾(K2FeO4)已经被广泛应用在水处理方面,高铁酸钾的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌的新型高效的多功能水处理剂。高铁酸钾在水处理过程中涉及到的过程正确的有:
①蛋白质的变性 ②蛋白质的盐析 ③胶体的聚沉 ④盐类水解 ⑤焰色反应 ⑥氧化还原反应
| A.①②③④ | B.①③④⑥ | C.②③④⑤ | D.②③⑤⑥ |
惰性电极电解下列溶液,电解一段时间,阴极质量增加,电解液的pH下降的是
| A.CuSO4 | B.NaCl | C.NaOH | D.H2SO4 |
下列各组热化学方程式中,化学反应的ΔH前者小于后者的是
①C(s)+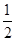 O2(g) ===CO(g);ΔH1C(s)+O2(g) ===CO2(g);ΔH2
O2(g) ===CO(g);ΔH1C(s)+O2(g) ===CO2(g);ΔH2
②S(g)+O2(g) ===SO2(g);ΔH3 S(s)+O2(g) ===SO2(g);ΔH4
③CaO(s)+H2O(l) ===Ca(OH)2(s);ΔH5 CaCO3(s) ===CaO(s)+CO2(g);ΔH6
| A.② | B.①② | C.①③ | D.②③ |
对于反应A2+3B2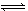 2C来说,以下表示的化学反应速率最快的是
2C来说,以下表示的化学反应速率最快的是
A.v (B2)="1.8" mol·L-1·min-1 B.v (A2)="0.4" mol·L-1·s-1
C.v (C)="0.6" mol·L-1·s-1 D.v (B2)="0.42" mol·L-1·s-1
下列说法正确的是
| A.CO能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应 |
| B.1 mol硫酸与1 mol Ba(OH)2完全中和所放出的热量为中和热 |
| C.相同条件下,2mol氢原子所具有的能量大于1mol氢分子所具有的能量 |
| D.101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 |
下列反应中生成物的总能量大于反应物总能量的非氧化还原反应是
| A.铝热反应 | B.氯化铝溶液的水解 |
| C.氢氧化钠和盐酸反应 | D.焦炭在高温下与水蒸气反应 |