(1)若40g密度为ρ g·cm-3的Ca(NO3)2溶液中含有4 g Ca(NO3)2,则溶液中NO的物质的量浓度为 mol/L
(2)在标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于1 L水中,所得溶液的密度为ρ g·cm-3,则此溶液的物质的量浓度为 mol/L
(3)NA代表阿伏加德罗常数。已知C2H4和C3H6的混合物的质量为a g,则该混合物所含共用电子对数目为_____,所含碳氢键数目为_____。
海洋是个巨大的资源宝库,海水资源的利用具有非常广阔的发展前景。海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下所示:
(1)步骤①反应的廊子方程式为_______________________________。
(2)步骤③反应的化学方程式为_________________________________。
(3)Br的原子序数是________,在周期表中位于第________周期、________族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:________________。
(5)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏,得出液溴?
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某些转化步骤及生成物未列出):
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是___________。
(2)上述流程中,工业上分离H2、CO2合理的方法是_____________________。
| A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸 |
| B.混合气加压冷却,使CO2液化 |
| C.混合气用氨水洗涤 |
| D.混合气先通入到石灰浆,然后高温煅烧固体 |
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行________,目的是________________;
在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法:________________。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
石油和煤炭加工过程涉及多种技术和设备。
(1)石油分馏时,在不断向________(填工业设备名称)内投放原料的同时获得产品,该过程为________操作过程。
(2)石油裂化分为热裂化、________和加氢裂化,裂化的目的是提高________的产量。
(3)煤的洗选是为了降低原煤中灰分和________的含量。煤的流化床燃烧是指空气从底部吹向煤炭颗粒,并使全部煤炭颗粒________进行燃烧的过程。
(4)煤的直接液化是煤与适当溶剂混合后在高温和________存在下与________作用生成液体燃料的过程。
有E、Q、T、X、Z五种前四周期元素,原子序数E<Q<T<X<Z。E、Q、T三种元素的基态原子具有相同的能层和能级,且I1(E)<I1(T)<I1(Q),其中基态Q原子的2p轨道处于半充满状态,且QT2+与ET2互为等电子体。X为周期表前四周期中电负性最小的元素,Z的原子序数为28。请回答下列问题(答题时如需表示具体元素,请用相应的元素符号):
(1)写出QT2+时的电子式:________,基态Z原子的核外电子排布式为________。
(2)Q的简单氢化物极易溶于T的简单氢化物,其主要原因有________等两种。
(3)化合物甲由T、X两元素组成,其晶胞如图1所示,甲的化学式为____。
(4)化合物乙的晶胞如图2所示,乙由E、Q两元素组成,硬度超过金刚石。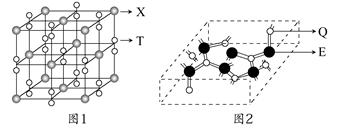
①乙的晶体类型为________,其硬度超过金刚石的原因是________。
②乙的晶体中E、Q两种元素原子的杂化方式均为________。
A、B、C、D、E、F六种元素的原子序数依次递增。
已知:①F的原子序数为25,其余的均为短周期元素;②元素A与元素B同周期,元素A与元素E同主族,且A、B、E三种原子p轨道上均有2个未成对电子;③元素C、D、E在同一周期,且C原子中没有未成对电子。
请回答下列问题:
(1)元素A与元素B的电负性大小比较为:________>________;元素C与元素D的第一电离能的大小比较为:________>________(填入相应的元素符号)
(2)F的核外电子排布式为________。
(3)元素B与元素E形成的晶体所属的晶体类型为________晶体,在该晶体中原子间形成的共价键属于________(从下列选项中选出正确类型)。
A.σ键 B.π键 C.既有σ键,又有π键
(4)由氢元素与A、B两元素共同构成的相对分子质量为30的分子里,中心原子的杂化轨道类型为________,分子的空间构型为________.
(5)根据等电子原理,写出由元素A与元素B构成的一种双原子极性分子的结构式:________。