从樟科植物枝叶提取的精油中含有下列甲、乙两种成分:

(1)乙中所含官能团的名称为 。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):

设计步骤①的目的是 ;指出①的反应类型 。
③反应的化学方程式为 (注明反应条件)。
(3)欲检验乙中的含氧官能团,选用下列的一种试剂是__________。
| A.溴水 | B.酸性高锰酸钾溶液 | C.溴的CCl4溶液 | D.银氨溶液 |
(4)乙经过氢化、氧化得到丙( 。丙的同分异构体中,既有苯环,又有羧基的共有 种。任意写出一种同时符合下列要求的丙的同分异构体结构简式_____________。
。丙的同分异构体中,既有苯环,又有羧基的共有 种。任意写出一种同时符合下列要求的丙的同分异构体结构简式_____________。
①能发生银镜反应;
②能与FeCl3溶液发生显色反应;
③核磁共振氢谱图上产生4个吸收峰。
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0)。试回答下列问题:
(1)写出反应过程中的离子反应方程式:OC段,
DE段,
EF段_______________________________________________________。
(2)硝酸溶液的物质的量浓度为mol·L-1
(3)B的值为_________mol,C的值为mL。
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素是(填元素名称)
(2)X与W组成的化合物中存在键(填“离子”、“共价”)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为 。
(4)由X、Y、Z、W四种元素可组成离子化合物A
①若1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条
件下A与NaOH溶液反应的离子方程式。
②若A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式
。
(5)由X、Y、Z、W和Fe五种元素组成的摩尔质量为392g/ mol的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量的浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为 。
② 已知100mL 1 mol/L 的B溶液能与20mL 1mol/L的酸性KMnO4溶液恰好反应。写出反应的离子方程式。
过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列
反应回答问题:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2↑+H2O
C.2H2O2=2H2O+O2↑
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)上述反应中,H2O2仅体现氧化性的反应是(填代号,下同),H2O2既体现氧化性又体现还原性的反应是,H2O2体现酸性的反应是。
(2)上述反应说明H2O2、Ag2O、K2CrO4的氧化性由强到弱的顺序是。
(3)保存过氧化氢试剂瓶上的最适合贴上的一个标签是(填序号);
(4)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2只发生了如下过程:H2O2→O2。
①反应体系选择的酸是:(填序号)。
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
②如果上述反应中有6.72L(标准状况)气体生成,转移的电子为mol。
(5)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的
氰化物(如KCN),经以下反应:KCN+H2O2+H2O=A+NH3↑,试指出生成物A的化学式为,并阐明H2O2被称为绿色氧化剂的理由是。
根据反应框图填空,已知反应①~⑤均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,B、D、J、L为气体。A是工业生产F的重要矿石原料的主要成份,其相对分子质量为120。
(1)I元素在元素周期表中的位置_______;M中阴离子的结构示意图:。
(2)固体A中所包含的化学键与固体Na2O2类似,则A的电子式为。
(3)写出反应①所使用设备的名称___________________。
(4)写出下列化学反应的离子方程式:
① 反应⑤:_________________________________________________;
② G与N的反应:________________________________________________;
③ K与L的反应:________________________________________________。
(5)已知每生成16 gD,放出106.5 kJ热量,则反应① 的热化学方程式为:
的热化学方程式为:
。
(1)在定量实验中,采用下列操作会导致实验结果偏低的是(填序号)。
A.中和热测定实验中以环形铁丝搅拌棒代替环形玻璃搅拌棒
B.配制100mL 2 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
C.测定硫酸铜晶体结晶水含量,加热并搅拌时,有少量固体溅出。
D.称取一定质量无水碳酸钠粉末,用稀盐酸滴定(用甲基橙作指示剂),测定盐酸浓度。酸式滴定管用蒸馏水润洗后未用待装液润洗,立即装液、滴定。
(2)下列实验操作或实验所得出的结论一定正确的是(填序号)
A.配制100mL 1.00mol/L的NaCl 溶液时,可用托盘天平准确称取5.85g NaCl
固体
B.某无色溶液中加入盐酸产生无色无味气体且能使澄清石灰水变混浊的气体,则
该溶液中一定含有大量的HCO3-
C.制备Fe(OH)3胶体时,应往沸水中加饱和的FeCl3溶液,并继续加热到溶液呈
红褐色为止
D.除去蛋白质中混有的少量NaCl,加AgNO3溶液后过滤
E.在中学“硫酸铜晶体里的结晶水含量的测定”实验中,至少需要进行四次称量操
作
F.测定中和热实验中,每次实验均应测量三个温度,即盐酸起始温度,NaOH溶液
的起始温度和反应后溶液的最高温度
(3)根据右图描述回答下列问题: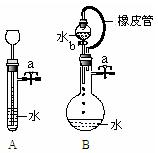
①关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示。试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)
②关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶。试判断:B装置是否漏气?
(填“漏气”、“不漏气”或“不能确定”),判断理由是。