(10分) 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:
2FeSO4 + a Na2O2 = 2Na2FeO4 + b X + 2Na2SO4 + c O2↑
①该反应中物质X应是 ,a与c的关系是 。
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式: 。
②每生成1mol FeO42-转移 mo1电子,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为 mo1。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题 。
(每空2分,共10分)
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、KCl等混合而成,为检验它们,做了如下实验:
①将固体混合物溶于水,搅拌后得无色透明溶液;
②往此溶液中滴加BaCl2溶液,有白色沉淀生成;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀全部溶解。
试判断:
(1)固体混合物中肯定有 ,肯定没有 ,可能有 。
(2)写出有关的离子方程式:实验② ;实验③ 。
(每空2分,共14分)
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
0.87 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
0.316 |
158 |
| 硝酸银 |
0.075 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是________________。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)配制1L上述“鲜花保鲜剂”所需的仪器有:量筒、玻璃棒、药匙、烧杯、__________、____________、___________。(在横线上填写所缺仪器的名称)需要高锰酸钾____________mol
(3)在溶液配制过程中,下列操作对配制结果没有影响的是_______________。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为_______________ mol/L。
(每空2分,共10分)
(1)同温同压下,若甲烷(CH4)和氨气(NH3)的体积相同,则质量比为 密度比 ;若二者含有的氢原子数相等,则它们的体积比为
(2)在___________mL 0.2 mol/L NaOH溶液中含2 g溶质;现在需要 45 mL 0.2 mol/L CuSO4溶液,配制时需要称量CuSO4·5H2O______________g。
现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子: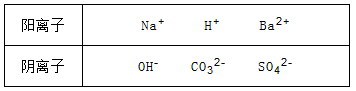
为鉴别它们,分别完成以下实验,其结果如下:
①A 溶液与B 溶液反 应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B 溶液与 C 溶液反应生成白色沉淀 D,沉淀 D 不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出下列物质的名称:X____________________。
(2)鉴别B在溶液中产生的阴离子的实验操作方法是______________________。
(3)完成以下水溶液中的反应的化学方程式:
A溶液与B溶液反应:_____________________
B溶液与E沉淀反应:_____________________
B与 C 反应至溶液呈中性:_____________________
(4)D 与 E 的混合物 ag,加入足量盐酸,反应完毕生成标准状况时的气体 bL,则D在混合物中的质量分数为___________________________。
(14 分)(1)某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图 1 所示。由图中可以看出,该同学在操作时的一个错误是_________________,烧杯的实际质量为_______________g。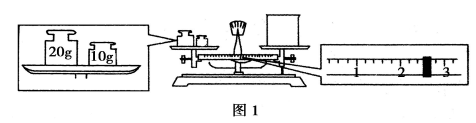
(2)需配制210 mL 0.2 mol·L-1 NaCl溶液,该同学转移溶液的示意图如图2所示。指出实验中存在的错误_______________________。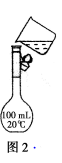
(3)用质量分数为 98%、密度为 1.84 g·cm-3的浓硫酸配制100 mL 0.1 mol·L-1的稀硫酸。
①应用量筒量取浓硫酸______________mL;
②配制硫酸时需用到的仪器有____________________________;(除量筒外,写出其余四种)
③下列操作使所配制溶液的物质的量浓度偏高的是____________(填序号)。
| A.称量时用了生锈的砝码 |
| B.将 NaOH 放在纸张上称量 |
| C.定容时俯视刻度线 |
| D.往容量瓶中转移时,有少量液体溅出 |
E.未洗涤溶解 NaOH 的烧杯
F.定容时仰视刻度线
G.容量瓶未干燥即用来配制溶液
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线