下列说法正确的个数是
①用四氯化碳萃取溴水中的溴,分液时有机层从分液漏斗的下端放出
②乙酸与乙醇的混合溶液可用分液漏斗进行分离
③在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
④利用饱和Na2CO3溶液能够除去二氧化碳中的氯化氢
⑤加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
⑥用溶解、过滤的方法分离KNO3和NaCl固体的混合物
⑦将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
| A.2 | B.3 | C.4 | D.5 |
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
如右图。反应中镁和铝的
| A.物质的量之比为3:2 | B.质量之比为2:3 |
| C.摩尔质量之比为2:3 | D.反应速率之比为3:2 |
右图是向100mL的盐酸中逐滴加入NaOH溶液时,混合溶液的pH变化图像,根据图像得出的结论正确的是
| A.原盐酸溶液的浓度为0.1mol/L |
| B.加入的NaOH溶液的浓度为0.1mol/L |
| C.至滴定终点用去NaOH为0.01mo1 |
| D.pH=12时,共加入NaOH溶液100mL |
下列有关实验的选项正确的是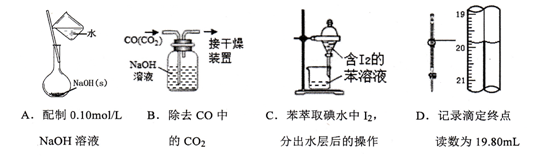
某老师批阅学生实验报告,下列哪些学生是以科学的态度记录实验数据的
| A.甲学生用50mL量筒量取46.70mL浓盐酸 |
| B.乙学生用广泛pH试纸测定溶液的酸碱性:pH=14.5 |
| C.丙学生配NaOH溶液,用电子天平称取固体1.220g |
| D.丁学生用酸式滴定管量取25.00mL 0.1mol/L的盐酸 |
右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是
| A.该硫酸的物质的量浓度为9.2mol/L |
| B.1mol Zn与足量该硫酸反应产生2g氢气 |
| C.配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL |
| D.该硫酸与等质量的水混合后所得溶液的浓度大于9.2mol/L |