某研究小组以粗盐和碳酸氢铵(NH4HCO3)为原料,采用以下流程制备纯碱(Na2CO3)和氯化铵(NH4Cl)。

已知盐的热分解温度:NH4HCO3 36℃;NaHCO3 270℃;NH4Cl 340℃;Na2CO3>850℃
请回答:
(1)从NaCl溶液到沉淀1的过程中,需蒸发浓缩。在加入固体NH4HCO3之前进行蒸发浓缩优于在加入NH4HCO3固体之后,其原因是 。
(2)为提高NH4Cl产品的产率和纯度,需在滤液1中加入氨水,理由是 ;步骤X包括的操作有 。
(3)测定NH4Cl产品的纯度时,可采用的方法:在NH4Cl溶液中加入甲醛使之生成游离酸(4NH4Cl+6HCHO=(CH2)6N4+4HCl+6H2O),然后以酚酞为指示剂,用NaOH标准溶液(需用邻苯二甲酸氢钾基准物标定)进行滴定。
①下列有关说法正确的是 。
| A.为了减少滴定误差,滴定管、锥形瓶均须用待装液润洗 |
| B.标准NaOH溶液可以装入带有耐腐蚀旋塞的玻璃滴定管中 |
| C.开始滴定前,不需擦去滴定管尖悬挂的液滴 |
| D.三次平行测定时,每次需将滴定管中的液面调至“0”刻度或“0”刻度以下的附近位置 |
②若用来标定NaOH标准溶液的邻苯二甲酸氢钾基准物使用前未烘至恒重,则测得NH4Cl产品的含量比实际含量 (填“偏大”、“偏小”或“无影响”)。
在①油脂②纤维素③蛋白质三种物质中,可用于制肥皂的是(填序号,下同),遇浓硝酸显黄色的是,可用于造纸的是。
下图是元素周期表的一部分,A、B、C、D、E、X是周期表给出元素组成的常见单质或化合物。
| ① |
|||||||||||||||||
| ④ |
⑤ |
⑥ |
|||||||||||||||
| ② |
⑦ |
||||||||||||||||
| Fe |
As |
||||||||||||||||
I.元素周期表是人们研究物质性质的重要工具
Y由②⑥⑦三种元素组成,它的水溶液是生活中常见的消毒剂。As可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为,当消耗1mol还原剂时,电子转移了 ________mol。
Ⅱ.已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
(1)若E为氧化物,则A的化学式为,A与水反应的化学方程式为,该反应中氧化剂和还原剂的物质的量之比为。
①当X是碱性盐溶液,C分子中有22个电子时,则C的结构式为,表示X呈碱性的离子方程式为。
②当X为金属单质时,则X与B的稀溶液反应生成C的离子反应方程式为
(2)若E为单质气体,D为白色沉淀,A的化学式可能是,B含有的化学键类为,C与X反应的离子方程式为。
(3)若B为单质气体,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,则该可逆反应的化学方程式为。t℃时,在密闭恒容的某容器中投入等物质的量的D和水蒸气,一段时间后达平衡,该温度下反应的平衡常数K=1,D的转化率为。
短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物,它们之间有图示的转化关系,已知C为密度最小的气体,甲俗称刚玉,是红宝石的主要成分。
⑴写出丙的名称:。
(2)写出下列变化的方程式:
①A与NaOH溶液反应的化学方程式。
②甲与NaOH溶液反应的离子方程式。
③乙溶液与过量CO2反应的离子方程式。
(3)甲的用途是(任写一种);A与Fe2O3的反应类型为。
短周期元素X、Y、Z、W原子序数依次增大。X是形成化合物种类最多的元素,Y是自然界含量最多的元素,Z是同周期中金属性最强的元素,W的负一价离子与Y的某种氢化物分子含有相同的电子数。
(1)元素X、Y、Z按原子半径由大到小的顺序排列为。(用元素符号表示)。
(2)W的单质与水反应的离子方程式为。
(3)化合物A由X、Y、Z三元素共同构成,其浓溶液中通入W的单质时,可产生气体XY2和化合物ZWY3。反应的化学方程式为。
A、B、C、D、E是Na的单质及其化合物,它们有如图所示的相互转化关系。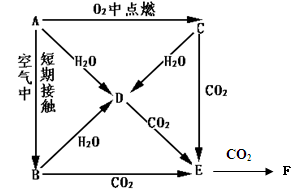
(1) 写出以下物质的化学式:CF
(2) 完成以下离子方程式:
C→D:
D→E:
(3) 等质量的A和B分别投入到等质量且足量的水中,反应后所得溶液溶质质量分数分别为
ω1、ω2,则ω1ω2 (填“>”或“<”或“==”)。
(4) E中混有少量的F,用化学方程式表示除去F的两种方法:
、
(5) 用m g的D来制取纯净的E,写出最简单的实验方法