在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g)  CO(g)+H2O(g)。
CO(g)+H2O(g)。
(1)已知在700 ℃时,该反应的平衡常数K1=0.5,则该温度下反应CO(g)+H2O(g)  CO2(g)+H2(g) 的平衡常数K2=________。
CO2(g)+H2(g) 的平衡常数K2=________。
(2)已知在1 000 ℃时,该反应的平衡常数K3为1.0,则该反应为__ ______反应(填“吸热”或“放热”)。
(3)能判断该反应达到化学平衡状态的依据是_________。(填编号)
| A.容器中压强不变 |
| B.c(CO2)=c(CO) |
| C.生成a mol CO2的同时消耗a mol H2 |
| D.混合气体的平均相对分子质量不变 |
(4)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v正_______v逆(填“>”、“=”或“<”),该温度下反应达到平衡时,CO2的转化率为_________。
在PH=1的硫酸溶液中,由水电离出的H+的物质的量浓度是。
在具有活塞的密闭容器中,一定温度下的可逆反应:

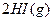 已达到平衡。将活塞外拉,则:
已达到平衡。将活塞外拉,则:
①容器内颜色②容器内压强
③逆反应速率④混合气体平均分子质量
(共11分).某反应中反应物与生成物有: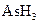 、
、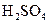 、
、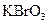 、
、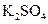 、
、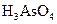 、
、 和一种未知物质X。(1)已知
和一种未知物质X。(1)已知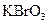 在反应中得到电子,则该反应的还原剂是。(2)已知0.2mol
在反应中得到电子,则该反应的还原剂是。(2)已知0.2mol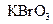 在反应中得到1mol电子生成X,则X的化学式为。(3)根据上述反应可推知。
在反应中得到1mol电子生成X,则X的化学式为。(3)根据上述反应可推知。
a.氧化性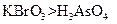 b.氧化性:
b.氧化性:
c.还原性: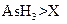 d.还原性:
d.还原性: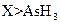
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目: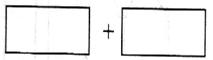
(共10分) A、B、C、D、E、F六种短周期元素的原子序数依次增大。
已知A、C、F三原子的最外层共有11个电子,且这种三元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个。试回答:
(1)写出下列元素的符号A ,D ,E 。
(2)用电子式表示B、F形成化合物的过程 。
(3)A、C两种元素最高价氧化物的水化物之间反应的离子方程式
(共6分)由氢气和氧气反应生成1 mol水蒸汽放热241.8kJ,写出该反应的热化学方
式 若1 g水蒸汽转化为液态水放热2.444kJ,则反应H2(g)+1/2O2(g)=H2O(l)的△H=__________kJ·mol-1,燃烧2mol氢气生成液态水能放出___________的热量。