用NaCl固体配制100mL 1.00mol•L﹣1NaCl溶液,不需要用到的仪器是
| A.100 mL容量瓶 | B.试管 | C.玻璃棒 | D.胶头滴管 |
下列实验装置、试剂选用或操作正确的是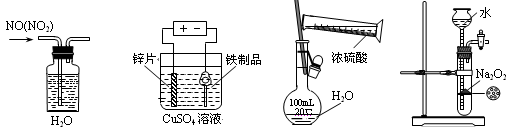
A .除去NO中的NO2B.铁制品表面镀锌 C.稀释浓硫酸 D.制备少量O2
.除去NO中的NO2B.铁制品表面镀锌 C.稀释浓硫酸 D.制备少量O2
短周期主族元素A、B、C、D原子序数依次增大。已知:A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是
A.原子半径:A< D< B < C B.A的氢化物稳定性大于C的氢化物稳定性
C.A在自然界中只能以化合态形式存在 D.D的单质可使干燥的红色布条褪色
在下列溶液中,各组离子一定能够大量共存的是
| A.常温下在酸度AG=lg〔c(H+)/c(OH-)〕=10的溶液中:Fe2+、K+、NO3-、SO42- |
| B.能溶解NH4HCO3固体产生气泡的溶液中:AlO2-、HCO3-、Ba2+、NO3- |
| C.使甲基橙变红的溶液中:NH4+ 、Na+、SO42-、Cl- |
| D.能使淀粉碘化钾试纸显蓝色的溶液:K+、NH4+ 、SO42-、S2- |
用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1molFeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 |
| B.标准状况下,1.12 L的HCHO所含的原子数是0.2NA |
| C.1 L0.5mol/LNa2CO3溶液中含有的CO32-数目为0.5NA |
| D.16.9 g过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA |
在恒温恒容的密闭容器中,发生反应 (注:x为P物质
(注:x为P物质
前的系数)①将3mol M和2 mol N在一定条件下反应,达平衡时P的体积分数为a;②若
起始时M、N、P投入的物质的量分别为n(M)、n(N)、n(P),平衡时P的体积分数也为a
则下列说法正确的是()
| A.若①达平衡时,再向容器中各增加l mol M、N、P,则N的转化率一定增大 |
| B.若向①平衡中再加入3mol M和2 mol N,P的体积分数若大于a,可判定x>4 |
| C.若x=2,则②体系起始物质的量应当满足3 n(N)=n(M) |
| D.若②体系起始物质的量满足3 n(P)+8 n(M)="12" n(N),可判定x=4 |