工业上电解饱和食盐水前,需要对食盐进行精制。已知工业食盐中含有Ca2+、Mg2+、SO42-等杂质。现欲把工业食盐精炼成精盐,请回答下列问题:
(1)欲除去SO42-必须加入可溶性的钡试剂,该试剂不可以是____________________。你选该试剂的理由是______________________。(共2分)
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)若选用的试剂是BaCl2、NaOH、Na2CO3和HCl,下列加入试剂的顺序不合理的是____________。
A.BaCl2、NaOH、Na2CO3、HCl
B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、NaOH、BaCl2、HCl
(3)在选用不同的试剂和不同的加试剂顺序时,都是最后加入盐酸。你认为加入盐酸的作用是(离子方程式表示_________________;__________________。(共4分)
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
(1)D的化学式(分子式)是_______________,E的化学式(分子式)是_______________。
(2)A和B反应生成C的化学方程式是
_______________________________________________。
(3)E和F反应生成D、H和G的化学方程式是
_______________________________________。
①—⑩分别代表有关反应物中的一种物质,请完成下列各题:
(1)①③④的化学式分别是__________________、___________________、_________________。
(2)⑧与⑨反应的化学方程式是
____________________________________________________。
有四瓶贴有标签的溶液,它们可能是碳酸钾、硝酸钡、硫酸氢钠和硫酸钾溶液。现进行有关实验,并记录部分现象。
(1)推断A是_____________、B是______________、C是______________、D是_____________。
(2)D和B反应的离子方程式是____________________________________________________。
(3)A和B反应的化学方程式是
_____________________________________________________。
硫酸亚铁是一种可用于医疗缺铁性贫血的药剂,硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的氧气氧化成硫酸铁(硫酸铁无治疗贫血的药效)。试设计一个实验以验证某硫酸亚铁药片是否被氧化(写出主要步骤、现象及有关的化学反应方程式) ____________________________________________。
我国南方饮用水大多为河水。由于河水中含有较多的泥沙、悬浮物、细菌等。在将河水用做饮用水之前需经下面A、B、C三步处理: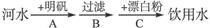
(1)A步中加入明矾的作用是____________________________________________。
(2)能够消毒杀菌的步骤是______________________________________________。
(3)可以除去较大颗粒、悬浮物的步骤是__________________________________。
(4)经过上述步骤,所得到的饮用水是___________(填“纯净物”或“混合物”),其原因是__________________________________________________________________。