在一定体积的密闭容器中,进行如下化学方程式:
CO(g)+H2O(g) CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.5 |
回答下列问题:
(1)该反应化学平衡常数的表达式为K= 。
(2)该反应为 (填“放热”或“吸热”)反应。
(3)能判断该反应是否达到化学平衡状态的依据是 。
A.容器中压强不变 B.混合气体中c(CO)不变
C.υ(正,H2)=υ(逆,H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O)。试判断此时的温度为 ℃。
Al及其化合物用途广泛,工业上可以将明矾石经处理后得到明矾[KAl(SO4)2·12H2O],再将明矾焙烧后制得Al2O3等物质,进一步处理后还可以得到Al。
已知焙烧明矾的化学方程式为:
请回答:
(1)Al2O3的摩尔质量是。
(2)工业上可用电解Al2O3制备Al,其化学方程式是。
(3)在焙烧明矾的反应中,氧化剂和还原剂的物质的量之比是。
(4)焙烧明矾时产生的SO2可综合利用来制硫酸。
已知25℃、101 kPa时:
2SO2(g) +O2(g) 2SO3(g)△H1 = 一197 kJ/mol
2SO3(g)△H1 = 一197 kJ/mol
2H2O (g)=2H2O(1)△H2 = 一44 kJ/mol
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3 = 一545 kJ/mol
SO3(g)与H2O(l)反应的热化学方程式是。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式。
②电池总反应的化学方程式。
工业上可用电解法来处理含Cr2O72-的酸性废水,最终可将Cr2O72-转化成Cr(OH)3沉淀而被除去。下图为电解装置示意图(电极材料分别为铁和石墨):
请回答:
(1)装置中的b电极是(填“阳极”或“阴极”)。
(2)a电极的电极反应式是。
(3)完成b电极附近溶液中反应的离子方程式:
Cr2O72-+6Fe2++14H+=2+6+7
(4)电解时用铁不用石墨做阳极的原因是。
(5)电解结束后,若要检验电解液中还有Fe2+存在,可选用的试剂是(填字母)。
| A.KSCN溶液 | B.CuCl2溶液 | C.H2O2溶液 | D.K3[Fe(CN)6] |
四种常见的短周期非金属元素在周期表中的相对位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的3倍。
| 甲 |
乙 |
|
| 丙 |
丁 |
请用化学用语回答:
(1)丙在元素周期表中的位置是___________。
(2)丁单质的电子式是_______________【(2)~(5)用化学用语回答】。
(3)乙的两种常见单质分别是。
(4)甲、丙、丁的气态氢化物水溶液显酸性的是___________。
(5)氢元素与甲和丁可以组成一种既有离子键、又有共价键的化合物,其化学式是。
(6)已知丁的非金属性比丙强,原因是_______________(从原子结构角度解释)。
结晶玫瑰是具有玫瑰香气的香料,可由下列方法合成(部分反应物及反应条件未标出)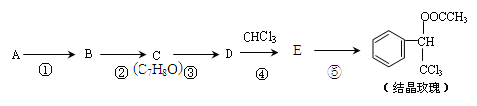
已知:  (-R表示烃基)
(-R表示烃基)
(1)A是苯的一种同系物,相同条件下,其蒸气对氢气的相对密度是46,则A的名称是。
(2)反应②所需药品及反应条件是。
(3)C的核磁共振氢谱峰面积之比是。
(4)⑤的化学方程式是。
(5)C有多种同分异构体,其中属于芳香族化合物的有种。
(13分)X、Y、Z、M、Q是中学化学常见的五种元素,原子序数依次增大,其结构或性质信息如下表:
| 元素 |
结构或性质信息 |
| X |
其原子最外层电子数是内层电子数的2倍 |
| Y |
基态原子最外层电子排布为nsnnpn+1 |
| Z |
非金属元素,其单质为固体,在氧气中燃烧时有明亮的蓝紫色火焰 |
| M |
单质在常温、常压下是气体。基态原子的M层上有1个未成对的p电子 |
| Q |
其与X形成的合金为目前用量最多的金属材料 |
(1)Q元素基态原子的电子排布式是:____________。
(2)比较Y元素与氧元素的第一电离能:____>____;X和Z形成的化合物XZ2为一种液体溶剂,其分子中的 键和
键和 键数目之比为:_____。
键数目之比为:_____。
(3)写出实验室制备M单质的离子方程式:_____。
(4)M的气态氢化物和氟化氢相比(写化学式):
稳定性强的是_____________,其原因是_____________________;
沸点高的是_____________,其原因是_____________________。