红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。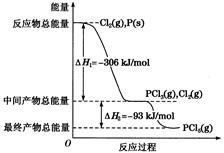
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是_______________________
(2)PCl5分解成PCl3和Cl2的热化学方程式是_______________________
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=__________________,P和Cl2一步反应生成1 mol PCl5的ΔH4_____________ΔH3(填“大于”、“小于”或“等于”)。
I、在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化。已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收249kJ的能量;形成水分子中 1mol H-O 键能够释放463kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在右边的横线上。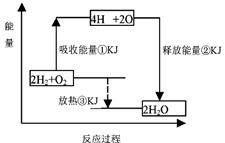
①kJ
②kJ
③kJ
II、二甲醚(CH3OCH3)是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。下图是二甲醚、乙烷燃烧过程的能量变化图: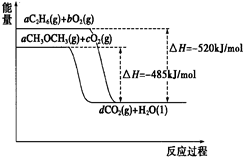
请回答下列问题:
(1)据图分析,a=;
(2)当有3g乙烷完全燃烧时,可放出热量Q =。
(3)请根据该图写出1mol二甲醚完全燃烧的热化学方程式。
利用生活中或实验室中常用的物品(电极材料、导线、电解质溶液、电流计),根据实验原理:Zn+2H+==Zn2++H2↑,根据选取材料自己动手设计一个原电池。
(1)选取的负极材料为,电解液为:
(2)电子由极经外电路流向极(填“正和负”)
(3)负极的电极反应式:。
(4)正极发生(“氧化”或“还原”)反应,周围会出现的现象是。
下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,化学性质最活泼的金属是。
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,碱性最强的是。
(3)③、④三种元素形成的离子,离子半径由大到小的顺序是。
(4)④和⑨两种元素形成化合物的化学式为,该化合物燃烧时的焰色为,该化合物溶液与元素⑧的单质反应的离子方程式为。
短周期元素X、Y、Z、W核电荷数依次增大,X、Z同主族,Z、W同周期,四种元素的原子序数之和为37,在周期表中X是原子半径最小的元素,Y的最外层电子数是内层电子数的3倍。
(1)W在周期表中的位置是第周期第族。
(2)X与Y 能形成具有18个电子的化合物,此化合物的电子式为。
(3)X、Y、Z三种元素组成的化合物中存在(填“化学键”名称)。
(4)Y、Z、W形成的某种化合物晶体类型是(填“晶体类型”名称)。
(5)X和Y形成的化合物沸点比X和W形成的化合物沸点(填“高”或“低”)。
(6)Z、W两种元素的最高价氧化物对应水化物溶液之间反应的离子方程式为。
现有①BaCl2②金刚石③碘片 ④冰 ⑤Na2SO4五种物质,按下列要求回答(填编号)
(1)熔化时不需要破坏化学键的是,熔化时需要破坏共价键的是;
(2)只有离子键的物质是,含有共价键的离子化合物是。