设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,5.6LCO2与足量Na2O2反应转移的电子数0.25NA |
| B.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
D.5NH4NO3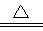 2HNO3↑+4N2+9H2O反应中,生成5.6gN2时,转移电子数目为3.75NA 2HNO3↑+4N2+9H2O反应中,生成5.6gN2时,转移电子数目为3.75NA |
原电池工作时()
| A.正极发生氧化反应 | B.负极发生氧化反应 |
| C.电子从正极流出 | D.负极质量一定减轻 |
下列说法正确的是
| A.凡是放热反应都是自发的,由于吸热反应都是非自发的 |
| B.自发反应一定是熵增大,非自发反应一定是熵减少或不变 |
| C.自发反应在恰当条件下才能实现 |
| D.自发反应在任何条件下都能实现 |
下列关于化学反应速率的说法中,不正确的是
| A.化学反应速率是衡量化学反应进行快慢程度的物理量 |
| B.在容积不变的反应器中,化学反应速率通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示 |
| C.对应化学反应来说,反应速率越大,反应现象就越明显 |
| D.化学反应速率是可以通过实验测定的 |
已知某反应的焓变小于零,则下列叙述正确的是()
| A.该反应一定是放热反应 |
| B.该反应一定是吸热反应 |
| C.该反应中反应物的总能量一定小于产物的总能量 |
| D.该反应需要加热才能发生 |
下列说法正确的是()
| A.需要加热才能发生的反应一定是吸热反应 |
| B.任何放热反应在常温条件下一定能发生反应 |
| C.反应物和生成物所具有的总能量决定了放热还是吸热 |
| D.吸热反应只能在加热的条件下才能进行 |