(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) △H1,平衡常数为K1;
FeO(s)+CO(g) △H1,平衡常数为K1;
反应Fe(s)+H2O(g) FeO(s)+H2(g) △H2,平衡常数为K2;在不同温度时K1、K2的值如下表:
FeO(s)+H2(g) △H2,平衡常数为K2;在不同温度时K1、K2的值如下表:
| |
700℃ |
900℃ |
| K1 |
1.47 |
2.15 |
| K2 |
2.38 |
1.67 |
①反应CO2(g)+ H2(g) CO(g)+ H2O(g) △H,平衡常数为K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g)+ H2(g)
CO(g)+ H2O(g) △H,平衡常数为K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g)+ H2(g) CO(g)+ H2O(g)是 反应(填“吸热”或“放热”)。
CO(g)+ H2O(g)是 反应(填“吸热”或“放热”)。
②能判断CO2(g)+ H2(g) CO(g)+ H2O(g)达到化学平衡状态的依据是 (填序号)。
CO(g)+ H2O(g)达到化学平衡状态的依据是 (填序号)。
A.容器中压强不
B.混合气体中c(CO)不变
C.v正(H2)= v逆(H2O
D.c(CO)= c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示。

①该条件下反应的平衡常数为 ;若铁粉足量,CO2的起始浓度为2.0mol·L-1,则平衡时CO2的浓度为____________mol·L-1。
②下列措施中能使平衡时 增大的是____________(填序号)。
增大的是____________(填序号)。
A.升高温度
B.增大压强
C.充入一定量的CO2
D.再加入一定量铁粉
现有m g某气体,它由四原子分子构成,它的摩尔质量为M g·mol-1。则:
(1)该气体的物质的量为________。
(2)该气体中所含的原子总数为________个。
(3)该气体在标准状况下的体积为________L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为________。
对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
(2)用CCl4提取溴水中的溴,可采用的方法。
(3)粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。对粗盐中的这些杂质可采用和的方法除去。
(4)除去氧化钙中的碳酸钙可用的方法。
现有①铁片 ②NaCl溶液③氨水④醋酸⑤酒精⑥盐酸 ⑦H2SO4
⑧KOH固体 ⑨蔗糖 ⑩KAl(SO4)2·12H2O,其中能导电的是,属于电解质的是_______,属于非电解质的是,属于酸的是,属于碱的是。(填序号)
美国化学家R.F.Heck因发现如下Heck反应而获得2010年诺贝尔化学奖。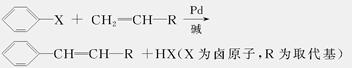

回答下列问题:
(1)C与浓H2SO4共热生成F,F能使酸性KMnO4溶液褪色,F的结构简式______。D在一定条件下反应生
成高分子化合物G,G的结构简式是___________________________。
(2)在A→B的反应中,检验A是否反应完全的试剂是_______________________________。
(3)E的一种同分异构体K符合下列条件:苯环上有两个取代基且苯环上只有两种不同化学环境的氢,与FeCl3溶液作用显紫色。K与过量NaOH溶液共热,发生反应的方程式为_________________________________________________________________________。
有机物A、B、C、D、E、F的转化关系如下: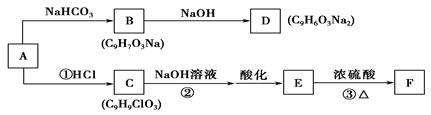
已知:①A是芳香族化合物,其苯环上有2个对位取代基,均不含支链,遇FeCl3溶液能发生显色反应。
②F分子中除了2个苯环外,还含有一个六元环。
请回答下列问题:
(1)A中含有________种官能团,A与足量溴水反应的化学方程式是_______________________。
(2)反应①~③中属于加成反应的有________(填序号)。
(3)C的结构简式为________________,F的结构简式为__________________。
(4)A→B的化学方程式是__________________________________________。