(1)取 300mL 0.2mol/L 的 KI 溶液与一定量的酸性 KMnO4溶液恰好反应,生成等物质的量的 I2 和 KIO3,则消耗 KMnO4 的物质的量的是 mol。
(2)在 Fe(NO3)3溶液中加入 Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 ,又变为棕黄色的原因是用离子方程式解释 。
(3)在 100mLFeBr2溶液中通入标况下2.24LCl2,溶液溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2 溶液中 FeBr2的物质的量浓度为 。
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式____ ___________________。向反应后的溶液中通入过量CO2,反应的离子方程式为________________。
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式 ,反应中生成0.2mol HNO3,转移的电子数目为 。②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是 。
用离子方程式表达下列应用或现象
(1)水垢的主要成分是碳酸钙和氢氧化镁,家庭中可用一定浓度的醋酸( CH3COOH)将其浸泡除去(任写一个即可)。
(2)向澄清石灰水中通二氧化碳气体变浑浊。
(3)小苏打治疗胃酸过多。
(4)向NaHSO4溶液中加入锌粉 。
。
测我国了“神舟”系列载人飞船的成功发射,标志着“炎黄子孙千年飞天梦想实现了”
(1)火箭升空时,由于与大气层的剧烈摩擦,产生高温。为了防止火箭温度过高,在火箭表面涂上一种特殊的涂料,该涂料的性质最可能的是_____(填写编号)。
| A.在高温下不融化 | B.在高温下可分解气化 |
| C.在常温下就分解气化 | D.该涂料不可能发生分解 |
(2)火箭升空需要高能的燃料,经常是用N2O4和N2H4作为燃料,其反应的方程式是:
N2O4 + N2H4 → N2 + H2O 。请配平该反应方程式:
+ H2O 。请配平该反应方程式:
————N2O4 + ————N2H4 → ————N2 + ————H2O
这个反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个很大的优点是 。
(3)为了向宇航员提供氧气,飞船上有专门的供氧装置。现有供氧剂过氧化钠与超氧化钾(KO2)。
①写出它们与二氧化碳反应的化学方程式(超氧化钾与二氧化碳的反应产物与过氧化钠类似): ___________________;_________________________。
②你选择的供氧剂是:_______________。
(6分)在有机溶剂里,使 与
与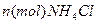 发生完全反应,释放出
发生完全反应,释放出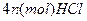 ,同时得到一种白色晶体A,A的熔点为113℃,在减压
,同时得到一种白色晶体A,A的熔点为113℃,在减压 时,50℃即可升华,测得A蒸气的密度(标准状况)为
时,50℃即可升华,测得A蒸气的密度(标准状况)为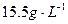 。
。
(1)通过计算得出A的化学式___________。
(2)生成A晶体的化学方程式为_____________。
(3)分子结构测定结果表明,同种元素的原子在A分子中所处的环境毫无差别,试写出A的结构式:____________。
(6分)标准状况下11.2L,由CO和 组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为_______;此混合气体完全燃烧消耗氧气的体积(标准状况)为___________L;将燃烧产物通过足量过氧化钠后,固体增重___________g。
组成的混合气体的质量为7.2g,则混合气体的平均摩尔质量为_______;此混合气体完全燃烧消耗氧气的体积(标准状况)为___________L;将燃烧产物通过足量过氧化钠后,固体增重___________g。
20.有关物质存在如下图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H。
请回答下列问题;
(1)反应①的化学方程式为;
(2)反应②的离子方程式为;
(3)写出另外一种实验室制取H的化学方程式;
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀.此沉淀的Ksp=7.1×10-9mol·L-3.将0.01 mol·L-1的D溶液与0.001 mol·L-1的Pb(NO3)2溶液等体积混合,你认为能否形成沉淀(填“能”或“不能”),请通过计算说明。