实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气。
(1)查阅资料。
20℃时不同质量分数硫酸的密度(g/mL)
| 质量 分数 |
0% (纯水) |
1% |
4% |
10% |
16% |
24% |
32% |
36% |
44% |
49% |
60% |
98% |
| 密度 |
1.00 |
1.01 |
1.02 |
1.07 |
1.11 |
1.17 |
1.24 |
1.27 |
1.34 |
1.39 |
1.50 |
1.84 |
分析以上数据,可以得出结论(写2条)
① ;② ;
(2)计算。
配制200g24.5%的稀硫酸,需 g98%浓硫酸和 g水。实际操作时,取98%浓硫酸 mL(精确到1mL);
(3)配制稀硫酸。分别用量筒量取所需水和浓硫酸,先将 倒入烧杯中,然后 ;若量取浓硫酸时俯视读数,会使稀硫酸的溶质质量分数 (填:偏大、偏小、不影响)
(6分)氯化钠是重要的调味品,下面三幅示意图分别表示不同的化学反应,但生成物中都有氯化钠。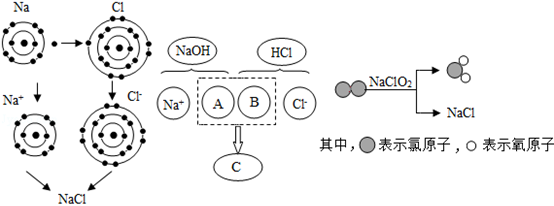
图1图2图3
(1)图1是钠与氯气反应生成氯化钠的微观示意图。由图1可知,元素的化学性质与(填字母序号)有密切的关系;
A. 最外层电子数 B. 内层电子数 C. 电子层数
(2)图2描述了NaOH溶液与盐酸反应的微观实质,图中A、B、C处应填入的化学式或离子符号依次为、、;
(3)图3表示反应的化学方程式为。
(5分)学习化学知识的目的之一是分析和解决实际问题。
(1)氢气是最清洁的燃料,其原因是 (用化学方程式表示);
(2)食品保鲜常采用真空包装或填充保护气。真空包装的目的是 ;
(3)下表为某品牌燕麦片标签中的一部分。
| 每100g含有营养成分 |
糖类 |
油脂 |
蛋白质 |
维生素C |
钙 |
镁 |
钠 |
锌 |
| 7.6g |
7.8g |
7.4g |
18mg |
201mg |
18.2mg |
30.8mg |
8.1mg |
①人类从食物中摄入的六大类主要营养素,上表出现了类;
②维生素C可溶于水,向其水溶液中滴入紫色石蕊溶液,变红色,加热该溶液至沸腾,红色消失。因此,烹调富含维生素C的食物时,应该注意。
(8分)下图是两套实验室制取气体的常用装置。
(1)制备CO2应选用的装置是(填编号),生成CO2的化学方程式为。
(2)B装置的气密性检查:先用止水夹夹住导管的橡皮管,然后向中加入水至形成一段水柱,静置,若观察到,说明装置不漏气。
(3)集气瓶中气体的检验:往集气瓶里加入,振荡,
若,说明该气体是CO2。
(4)收集到一瓶二氧化碳后,按下图所示进行实验,观察到的现象是。
(1)实验室测定溶液pH值,除了使用到pH试纸和白瓷板之外,还需要的仪器是_________
(2)过滤实验中,过滤后的液体浑浊,经检查发现滤纸破损,你应该要进行的处理是_______________。
金属镍(Ni)与铁具有相似的化学性质。
(1)镍可形成化合价为+2和+3的两种氧化物,它们的化学式分别是、。
(2)氢氧化镍Ni(OH)2为强碱,请写出它与稀盐酸反应的化学方程式 。
(3)已知:正二价镍离子Ni2+显绿色。将金属镍投入稀盐酸中,发生反应的化学方程式为
Ni + 2HCl = NiCl2 + H2↑,则预测可观察到的现象是,
产生该现象的原因是溶液中离子减少,离子增加。