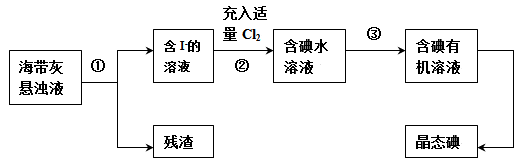
海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:
(1)灼烧海带时需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
A.烧杯 B.蒸发皿 C.坩埚 D.干燥器
(2)指出上图中提取碘的过程中有关的实验操作名称:① ,③ 。
(3)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50ml碘水和15ml有机溶剂(你所选的)加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E. 旋开活塞,用烧杯接收溶液;
F. 从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
过程③正确操作步骤的顺序是:(填编号字母) ;
(4)从含碘的有机溶液中提取碘和回收有机试剂,还需要经过蒸馏,观察下图所示实验装置指出其错误 。
(5)进行上述蒸馏操作时,最后晶态碘在____________(填仪器名称)里聚集。
(10分)某同学为研究氧化铁与过量炭粉的反应,进行如下实验:
①称取3.2 g氧化铁与2 g炭粉均匀混合,放入48.48 g的玻璃管中,按如图装置连接。
②通一段时间纯净、干燥的氮气。
③夹紧T处弹簧夹,然后点燃酒精灯,加热一段时间后,澄清石灰水变浑浊。
④完全反应后,冷却至室温,称得玻璃管和固体的总质量为52.24g。
⑴实验步骤①加入药品前,先进行的操作是。
⑵实验步骤②通入N2的目的是,实验室可以用氯化铵饱和溶液和亚硝酸钠饱和溶液混合加热反应制得氮气。请写出该反应的离子方程式:_____________________________________________________________。
⑶经计算,参加反应的碳元素质量为 g。
⑷反应生成的气体是______________________,
该实验的化学方程式为:__________________________________________________。
⑸该实验设计存在不合理之处,请指出并说明改进方法 _________
_______________________________________________________________________。
(9分)酸碱中和滴定是中学化学常见实验。
某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
| A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。 |
| B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。 |
| C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。 |
| D.将物质的量浓度为1.50mol/L标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。 |
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水稀释。
H.重复以上实验。
请回答下列问题:
(1)该实验正确操作步骤的顺序为 → A→ → →D→ → → H
(用编号字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。滴定过程中,视线应注视 ;判断到达滴定终点的现象是 。
(4)下表是实验测得的有关数据:
| 滴定序号 |
待测稀硫酸的体积(mL) |
所消耗NaOH标准溶液液的体积(mL) |
|
| V1 |
V2 |
||
| ① |
20.00 |
0.50 |
22.60 |
| ② |
20.00 |
6.00 |
27.90 |
请计算出该浓硫酸样品的浓度为 mol·L-1(不必写出计算过程)。
有一固体混合物,可能由Na2CO3、Na2SO4、FeSO4、CaCl2、NaCl等混合而成,为检验它们,做了以下实验:
①将固体混合物溶于水中,搅拌后得无色透明溶液;
②往此溶液中滴加硝酸钡溶液,有白色沉淀产生;
③过滤,将沉淀物置于稀硝酸中,发现沉淀部分溶解。
根据上述实验事实,回答下列问题:
(1)原固体混合物中一定含有的物质是,一定不含有的物质是,可能含有的物质是(以上空格均填写化学式)。对可能含有的物质,可采用向滤液中滴加溶液的方法来检验。
(2)写出步骤③中的离子方程式。
为了证明一水合氨是弱电解质,甲、乙、丙、丁四位同学利用下面的
试剂进行实验:0.10 mol·L-1氨水、NH4Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸
馏水。
(1)甲用pH试纸测出0.10 mol·L-1氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论________(填“正确”、“不正确”或“无法确定”),并说明理由____________________________________。
(2)乙取出10 mL 0.10 mol·L-1氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至
1 000 mL,再用pH试纸测出其pH为b,他认为只要a、b满足如下关系________(用等式或不等式表示)就可以确认一水合氨是弱电解质。
(3)丙取出10 mL 0.10 mol·L-1氨水,滴入2滴酚酞试液,显粉红色,再加入CH3COONH4晶体少量,颜色变浅;你认为这一方法能否证明一水合氨是弱电解质,________(填“能”或“否”)。
(4)丁同学的方案最可能是(答出实验操作方法、现象与结论)_____________________。
丁同学的方案的原理为(用离子方程式表示)_____________________。
某学生用下图的装置进行一氧化碳和二氧化碳混合气体的分离和干燥。其中a为铁夹,b为分液漏斗的活塞。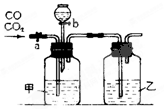
(1)甲瓶内盛溶液,乙瓶内盛溶液,分液漏斗内盛溶液。
(2)实验先分离出一氧化碳,方法是先关闭,再打开。
(3)分离完一氧化碳后,再收集二氧化碳,方法是先关闭,再打开。