目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g) ,CO2(g)和H2O(l)的热化学方程 式_____________________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下
N2(g)+CO2(g)某研究小组向恒容密闭容器加入一定量的活性炭和NO,恒温(T。C)条件下反应,反应进行到不同时间测得各物质的浓度如下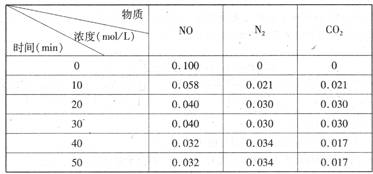
①不能作为判断反应达到化学平衡状态的依据是______________
A.容器内CO2的浓度保持不变
B.v正(N2)="2" v正(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②在T。C时.该反应的平衡常数为______________(保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是______________
(3)甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解50ml2mol/L的氯化铜溶液的装置示意图:
请回答:
①甲烷燃料电池的负极反应式是:__________________________。
②当A中消耗0.05mol氧气时,B中________________极(填“a”或“b”)增重________________g。
按要求回答下列各题:
(1)某原子质子数为16,写出该原子的结构示意图;
(2)某一价阳离子的核外电子排布与Ne相同,写出该离子的结构示意图;
(3)核内中子数为N的R2+,质量数为A,则该离子的核外电子数为。
按要求完成下列各题:
(1)写出下列物质在水溶液中的电离方程式
H2SO4;MgCl2;NaHCO3;
(2)现代工业上用电解饱和食盐水的方法制取Cl2,反应的化学方程式为____________________
从一个关系量的单位,我们可以得出该量的计算公式,如:从摩尔质量的单位:g·mol-1,可得出分子应当是质量、分母应当是物质的量,因此摩尔质量的计算公式为 M = m / n,以此类推,物质的量浓度单位是,其计算公式c = ;
由微粒个数与物质的量的关系推出阿佛加德罗常数的公式NA= ;
气体摩尔体积的单位是,其计算公式是Vm= 。
0.1mol H2S共有约mol电子,17g NH3共有个电子。同温同压下,同体积的NH3和H2S气体气体的质量之比为;同温同压下,同质量的NH3和H2S气体的体积比为;氢原子的个数比为
在mol Al2(SO4)3中含0.3molSO42-,其中含Al3+mol。在2L的0.5mol/LNa2SO4溶液中含有molNa+,molSO42-,c(Na+)为mol/L,其中Na2SO4的质量为g。