铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述________________(填装置序号)装置原理进行防护;装置③中总反应的离子方程式为______________________。
(2)用CH4或其他有机物、O2为原料可设计成原电池,以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为___________________________。
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。
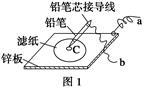

图2电池负极区的电极反应为_________________________;若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则滤纸出现_____________色,C位置的电极反应式为___________________若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是__________(填A或B)电极。
(4)广西治理龙江河镉(Cd2+)污染时,先向河中投入沉淀剂将Cd2+转化为难溶物,再投入氯化铝,试说明氯化铝的作用_______________________________(用必要的离子方程式和文字进行解释)。
Ⅰ.现有标准状况下的以下物质:
| A.11.2LO2 | B.6.8gNH3 | C.1.204×1024CH4 | D.0.5molCO2; |
其中质量由大到小的顺序为,
各物质所含原子数由大到小的顺序是,
其体积由大到小的顺序是,
气体的密度由大到小的顺序是。(填序号)
Ⅱ.相同质量的CO和CO2,其物质的量之比为,所含的氧原子个数比为,所含碳元素的质量比为,相同条件下的体积比为。
火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋 发图强。黑火药在发生爆炸时,发生如下的反应:
2KNO3+3C+S===K2S+N2↑+3CO2↑。
其中(1)被还原的元素是,被氧化的元素是,
(2)还原剂是,还原产物是。
(3)当2molKNO3发生反应时,生成的氧化产物的物质的量为mol。
根据下列数据判断元素X的相对原子质量
(1)1.01*105Pa,273K时气态单质Xn的密度为d g/L,则X的相对原子质量为____________
(2)相同状况下,一定体积的X的气态氢化物HmX的质量是等体积NH3的2倍,则X的相对原子质量_________________________
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为________________________
一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液) + 3O2(气) = XO2(气) + 2YO2(气)冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是_ ______________。
②化合物XY2的摩尔质量是____________________。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_________和________。(写元素符号)
下列各组混合物的分离或提纯应采用什么方法最合适?
(1)除去Ca(OH)2溶液中悬浮的CaCO3颗粒,用方法;
(2)除去乙醇中溶解的微量食盐,用方法;
(3)除去氧化钙中的碳酸钙,用方法;
(4)提取碘水中的碘,用方法;
(5)除去食盐溶液中的水,可采用方法