已知25℃时:①HF(aq)+OH-(aq) F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
②H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol下列有关说法中正确的是
A.HF电离:HF(aq) H+(aq)+F-(aq)△H=+10.4KJ/mol H+(aq)+F-(aq)△H=+10.4KJ/mol |
| B.水解消耗0.1 mol F-时,吸收的热量为6.77 kJ |
| C.中和热均为57.3 kJ/mol |
| D.含0.1 mol HF、0.1 mol NaOH的两种溶液混合后放出的热量为6.77 kJ |
1987年2月,朱经武教授等发现钇钡铜氧化合物在90 K下即具有超导性,若该化合物的基本结构单元如图1-22所示,则该化合物的化学式可能是()
图1-22
| A.YBa2CuO7-x |
| B.YBa2Cu2O7-x |
| C.YBa2Cu3O7-x |
| D.YBa2Cu4O7-x |
下列指定粒子的个数比为2∶1的是()
| A.Be2+中的质子和电子 |
B.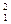 H原子中的中子和质子 H原子中的中子和质子 |
| C.NaHCO3晶体中的阳离子和阴离子 |
| D.BaO2(过氧化钡)固体中的阴离子和阳离子 |
科学界拟合成一种“双重结构”的球形分子,即把足球烯C60分子容纳在Si60分子中,外面的硅原子与里面的碳原子以共价键结合,下列有关叙述正确的是()
| A.该反应属于置换反应 |
| B.该晶体属于原子晶体 |
| C.该物质具有极高的熔沸点 |
| D.该物质是一种新型化合物 |
经研究发现,有一种磷分子具有链状结构,其组成可以表示为 。
。
有关它的叙述正确的是()
①它易溶于水②它与白磷互为同素异形体③它的相对分子质量是白磷的8倍④其分子中具有不饱和键⑤其分子中每个磷原子以非极性键与另外3个磷原子结合
| A.①②③ | B.②③⑤ |
| C.①③⑤ | D.②③④ |
美国科学家成功地在高压下将CO2转化成具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体的说法正确的是()
| A.CO2的原子晶体和分子晶体互为同素异形体 |
| B.在一定条件下,CO2分子晶体转化为原子晶体是物理变化 |
| C.CO2的原子晶体和CO2的分子晶体具有相同的物理性质 |
| D.在CO2的原子晶体中,每一个C原子周围结合4个O原了,每一个O原子跟2个C原子结合 |