(6分)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO的浓度,某兴趣小组提出以下两种方案:
a.在微碱性条件下,用Fe(OH)2还原NO3-,还原产物为NH3;
b.在碱性条件下,用铝粉还原NO3-,还原产物为N2。
(1)方案a中,生成34g NH3的同时生成__________mol Fe(OH)3。
(2)方案b中发生的反应如下(配平该反应离子方程式):
______Al+______NO3-+______OH-===______AlO2-+______N2↑+______H2O
(3)方案b中,当有0.15 mol电子转移时,生成的氮气在标准状况下的体积为_________mL。
“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为N2O与CO2分子具有相似的结构(包括电子式);又已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为__________,由此可知它__________ (填“含有”或“不含”)非极性键。
氮可以形成多种离子,如N3-、NH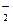 、N
、N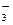 、NH
、NH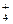 、N2H
、N2H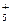 、N2H
、N2H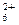 等,已知N2H
等,已知N2H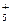 与N2H
与N2H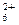 是由中性分子结合质子形成的,类似于NH
是由中性分子结合质子形成的,类似于NH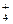 ,因此有类似于NH
,因此有类似于NH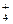 的性质。
的性质。
(1)NH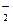 的电子式为__________。
的电子式为__________。
(2)N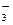 有__________个电子。
有__________个电子。
(3)写出两种由多个原子组成的含有与N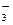 电子数相同的物质的化学式__________。
电子数相同的物质的化学式__________。
(4)等电子数的粒子往往具有相似的结构,试预测N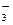 的构型____________________。
的构型____________________。
(5)据报道,美国科学家卡尔·克里斯特于1998年11月合成了一种名为“N5”的物质,由于其具有极强的爆炸性,又称为“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键。则“N5”分子碎片所带电荷是__________。
W、X、Y、Z四种短周期元素的原子序数X>W>Z>Y。W原子的最外层没有p电子,X原子核外s电子与p电子数之比为1∶1,Y原子最外层s电子与p电子数之比为1∶1,Z原子核外电子中p电子数比Y原子多2个。
(1)X元素的单质与Z、Y所形成的化合物反应,其化学方程式:________________________。
(2)W、X元素的最高价氧化物对应水化物的碱性强弱为__________<__________(用分子式表示)。
(3)这四种元素原子半径的大小为__________>__________>__________>__________(填元素符号)。
有第四周期的A、B、C、D四种元素,其价电子数依次为1、2、2、7,其原子序数依A、B、C、D依次增大。已知A与B的次外层电子数为8,而C与D为18。根据原子结构,判断:
(1)哪些是金属元素?__________。
(2)D与A的简单离子是 __________。
(3)__________元素的氢氧化物碱性最强。
(4)B与D的两原子间能形成的化合物是____________________(写出化学式)。
有机物
是最常用的食用油氧化剂,分子式为
,可发生如下转化:



 已知
的相对分子质量为60,分子中只含一个甲基。
的结构可表示为:
已知
的相对分子质量为60,分子中只含一个甲基。
的结构可表示为:

 请回答下列问题:
请回答下列问题: (1)根据系统命名法,
的名称为。
(1)根据系统命名法,
的名称为。 (2)官能团
的名称为,高聚物
的链节为。
(2)官能团
的名称为,高聚物
的链节为。 (3)
的结构简式为。
(3)
的结构简式为。 (4)反应⑤的化学方程式为。
(4)反应⑤的化学方程式为。 (5)
有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式。
(5)
有多种同分异构体,写出期中2种符合下列要求的同分异构体的结构简式。 i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应
i.含有苯环 ii.能发生银镜反应 iii.不能发生水解反应 (6)从分子结构上看,
具有抗氧化作用的主要原因是(填序号)。
(6)从分子结构上看,
具有抗氧化作用的主要原因是(填序号)。 a.含有苯环 b.含有羰基c.含有酚羟基
a.含有苯环 b.含有羰基c.含有酚羟基