A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐.它们的转化关系如图所示.请回答:
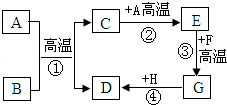
(1)物质B、E和F的化学式为B 、E 、F ;
(2)反应①的化学方程式为: ,其反应类型为 。
B、D是常见金属单质,A是一种红棕色金属氧化物,电解熔融态的C得到B单质,J是一种难溶于水的白色固体。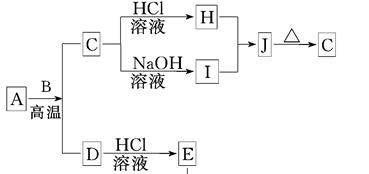
(1)在E的溶液中加入氢氧化钠溶液,可以观察到的现象是________________________.
(2)按要求写化学方程式或离子方程式:
①A与B在高温条件下生成C和D的化学方程式:____________________________;
②在E的水溶液中通入氯气后的生成物和I溶液反应的离子方程式:。
(3)由D和A组成的混合物与稀HCl作用,固体恰好溶解,所得溶液中滴加KSCN溶液不显红色,且生成的E与H2的物质的量之比为4:1。则反应物中A、D、HCl的物质的量之比为____。
A—J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕色固体。
请回答下列问题:做无机推断题找到突破点是关键,A是一种高熔点物质,可知A为Al2O3,D是一种红棕色固体,可知D为Fe2O3,B为O2,C为Al,E为Fe,F为FeCl2,G为Fe(OH)2,J为Fe(OH)3,H为NaAlO2,I为AlCl3。
(1)电解A物质的阳极电极反应式为___________,C与D在高温下反应,引发该反应需要加入的一种试剂是____________________(写化学式)
(2)写出G→J反应的实验现象与化学方程式____________________________________,__________________________________
(3)H 与I反应的离子方程式为___________________________________________
(4)用离子方程式表示I物质能用于净水的原理___________________________________
下面是以化合物I为原料合成一种香精(化合物VI)的合成路线,反应在一定条件下进行。化合物Ⅵ广泛用于香精的调香剂。
回答下列问题:
(1)化合物Ⅰ生成化合物Ⅱ的反应原子利用率可达100%,化合物Ⅰ的名称为。化合物II生成化合物III的反应条件为____________,
(2)化合物VI生成化合物VII的反应类型为。化合物III生成化合物IV可能的中间产物的结构简式为______________________。
(3)写出化合物Ⅴ生成化合物VI的反应方程式: ________(4)化合物V的同分异构体中,与化合物V官能团种类相同且无支链的化合物有多种,写出其具有顺反异构的同分异构体的顺式结构简式、。
中学常见的单质A、B、C(其中A为金属单质)和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲是电解质。
根据以上转化关系回答:
(1)写出下列物质的化学式:
A: ;B: ;乙: ;丁: 。
(2)①A与NaOH溶液反应的化学方程式: 。
②乙与过量的CO2反应的离子方程式: 。
已知有以下物质相互转化
试回答:
(1)写出B的化学式,D的化学式。
(2)写出由E转变成F的化学方程式。
(3)向G溶液加入A的有关离子反应方程式。