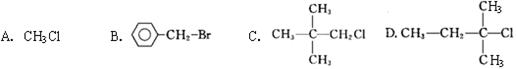地壳中含量最多的金属元素和含量最多的非金属元素所形成的化合物是
| A.Fe3O4 | B.Al2O3 | C.SiO2 | D.CuO |
绿色化学提倡化工生产应提高原子利用率。原子利用率表示目标产物的质量与生成物总质量之比。在下列制备环氧乙烷反应中,原子利用率最高的是



如下图,在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为
| A.十二面体 | B.正八面体 | C.正六面体 | D.正四面体 |
HgCl2的稀溶液可用作手术刀的消毒剂,已知HgCl2的熔点是277 ℃,熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力,则下列关于HgCl2的叙述中正确的是
①HgCl2属于共价化合物 ②HgCl2属于离子化合物 ③HgCl2属于非电解质 ④HgCl2属于弱电解质
| A.①③ | B.①④ | C.②③ | D.②④ |
物质的下列性质不能用键能来解释的是
| A.氮气的化学性质没有氯气活泼 | B.HF比HCl稳定 |
| C.金刚石的熔点比晶体硅高 | D.常温下溴呈液态,碘呈固态 |
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是